题目内容
【题目】请根据下列实验图示回答下列问题。

(1)实验室用过氧化氢溶液和二氧化锰制取氧气,写出反应的化学方程式是___________。
(2)小明同学用30%的过氧化氢溶液和二氧化锰制取氧气,发现放出氧气的速率太快,原因是_________________________________________,用A装置来制取氧气,还是不能得到平稳的氧气流,经讨论将发生装置由A改为B,其理由是_____________________。
(3)用C装置收集氧气的最佳时机是_______________________________________。
(4)D实验中硬质玻璃管中的现象是_______,写出反应的化学方程式是__________。
从环保的角度考虑,装置有不足之处,改进措施是____________________。
(5)E实验中,若要除去粗盐中难溶性的杂质其操作步骤为____________(填序号),步骤⑤中玻璃棒的作用是________________________,若按照②③①的步骤配置50g质量分数为16%的氯化钠溶液所配置溶液的质量分数(填“偏大”或“偏小”)___________。
若②出现了右盘低的现象操作应该是__________________。
a.左边的平衡螺母向左调 b.右边的平衡螺母向右调 c.右盘中减少砝码 d.左盘中增加食盐
【答案】 2H2O2![]() 2H20+O2↑ 过氧化氢溶液的浓度太大(或把二氧化锰加入到了过氧化氢溶液中) 控制液体的流速 当有均匀连续气泡产生时 红棕色粉末逐渐变黑 3CO+Fe2O3
2H20+O2↑ 过氧化氢溶液的浓度太大(或把二氧化锰加入到了过氧化氢溶液中) 控制液体的流速 当有均匀连续气泡产生时 红棕色粉末逐渐变黑 3CO+Fe2O3![]() 2Fe+3CO2 在导管a处放一盏燃着的酒精灯 ①④⑤ 搅拌,防止局部温度过高液滴飞溅 偏小 d
2Fe+3CO2 在导管a处放一盏燃着的酒精灯 ①④⑤ 搅拌,防止局部温度过高液滴飞溅 偏小 d
【解析】(1). 过氧化氢溶液在二氧化锰的作用下分解生成水和氧气,反应方程式为:2H2O2![]() 2H20+O2↑ (2). 反应物的浓度越高,反应越快,放出氧气的速率太快,原因是过氧化氢溶液的浓度太大(或把二氧化锰加入到了过氧化氢溶液中) (3). 用注射器添加液体试剂,可以控制液体的滴加的速率,进而控制反应速率 (4). 当有均匀连续气泡产生时,开始收集气体,如果开始冒气泡时,导管导出的是装置中的空气,此时就收集,导致收集的气体不纯; (5). 氧化铁和一氧化碳反应生成铁和二氧化碳;氧化铁是红棕色固体,铁粉是黑色固体,所以可观察到:红棕色粉末逐渐变黑 (6). 氧化铁和一氧化碳的反应方程式为: 3CO+Fe2O3
2H20+O2↑ (2). 反应物的浓度越高,反应越快,放出氧气的速率太快,原因是过氧化氢溶液的浓度太大(或把二氧化锰加入到了过氧化氢溶液中) (3). 用注射器添加液体试剂,可以控制液体的滴加的速率,进而控制反应速率 (4). 当有均匀连续气泡产生时,开始收集气体,如果开始冒气泡时,导管导出的是装置中的空气,此时就收集,导致收集的气体不纯; (5). 氧化铁和一氧化碳反应生成铁和二氧化碳;氧化铁是红棕色固体,铁粉是黑色固体,所以可观察到:红棕色粉末逐渐变黑 (6). 氧化铁和一氧化碳的反应方程式为: 3CO+Fe2O3![]() 2Fe+3CO2 (7). 在导管a处放一盏燃着的酒精灯,将尾气中的一氧化碳点燃,防止污染空气; (8). 粗盐提纯选的操作有:溶解、过滤、蒸发结晶 (9). 蒸发时,玻璃棒的作用是搅拌,使液体受热均匀,防止局部温度过高液滴飞溅 (10).量取液体时,仰视读数,读数偏小,实际液体的量偏多,导致配制溶液的溶质质量分数 偏小 (11). 若②出现了右盘低的现象,说明所加固体的量少,没有达到想要的数值,操作应该是左盘中增加食盐至天平平衡。
2Fe+3CO2 (7). 在导管a处放一盏燃着的酒精灯,将尾气中的一氧化碳点燃,防止污染空气; (8). 粗盐提纯选的操作有:溶解、过滤、蒸发结晶 (9). 蒸发时,玻璃棒的作用是搅拌,使液体受热均匀,防止局部温度过高液滴飞溅 (10).量取液体时,仰视读数,读数偏小,实际液体的量偏多,导致配制溶液的溶质质量分数 偏小 (11). 若②出现了右盘低的现象,说明所加固体的量少,没有达到想要的数值,操作应该是左盘中增加食盐至天平平衡。

【题目】 如图是某燃气热水器的内部构造示意图。
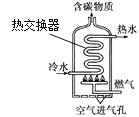
(1)若该热水器采用天然气为燃气。
①写出天然气的主要成分完全燃烧的化学方程式:______;
②当“空气进气孔”部分堵塞,燃料不完全燃烧时产生有毒的__气体;
③燃气热水器中的热交换器采用了回形管结构,它的优点是______。
(2)热值是指1kg某种燃料完全燃烧放出的热量,常见三种燃料的热值及1kg燃料燃烧产生的CO2和SO2的质量如下表。
燃料 | 热值kJ/kg | 燃烧产物的质量/g | |
二氧化碳 | 二氧化硫 | ||
汽油 | 约48000 | 2900 | 5.0 |
天然气 | 约56000 | 2500 | 0.1 |
煤 | 约33000 | 2500 | 11.0 |
结合上表数据分析:以上三种燃料中最清洁高效的能源是______,理由是______。