题目内容
【题目】如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题。
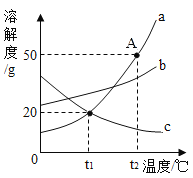
(1)A点的含义是_____________________________。
(2)气体的溶解度随温度的变化规律与__________(填“a”、“b”或“c”)相似。
(3)若使a、c的饱和溶液同时析出晶体,方法是___________。
(4)在t2℃时,a、b、c三种饱和溶液降温至t1℃时溶质的质量分数由大到小的顺序是_____________________。
【答案】在t2℃时a物质的溶解度是50g c 蒸发溶剂 b>a>c
【解析】
(1)根据溶解度曲线可知,A点表示在t2℃时a物质的溶解度是50g;
(2)气体溶解度随温度的升高而减小,故气体的溶解度随温度的变化规律与c相似,故填:c;
(3)使a、c的饱和溶液同时析出晶体,需要采用蒸发溶剂的方法;
(4)将t2℃时a、b、c三种物质的饱和溶液降温到t1℃时,a、b的溶解度减小,c的溶解度随温度的降低而增大,a、b有晶体析出,质量分数变小溶液仍为饱和溶液,c没有晶体析出,质量分数不变,一定温度下饱和溶液的溶质质量分数=![]() ,溶解度越大,质量分数越大,t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以t1℃时三种物质的溶质质量分数由大到小的顺序是b>a>c。
,溶解度越大,质量分数越大,t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以t1℃时三种物质的溶质质量分数由大到小的顺序是b>a>c。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】实验室现有硫酸铜和硫酸钠的固体混合物样品,小明同学想测定样品中硫酸铜的质量分数。先称取该混合物样品25g,完全溶于水中,然后取用了一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
次数/物质的质量 | 1 | 2 | 3 | 4 |
加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
生成沉淀的质量/g | 4.9 | x | 14.7 | 14.7 |
(1)表中X的数值为________________;
(2)计算原固体混合物样品中硫酸铜的质量分数为___________?
(3)上述实验中所用到的氢氧化钠溶液,是小海同学利用实验室中已有的80g溶质质量分数为40%的氢氧化钠溶液配置的,计算需加入______克水(只写计算结果),才能配成实验中所需溶质质量分数的氢氧化钠溶液.
【题目】下列化学知识归纳整理的相关内容中完全正确的一组是:
A.数轴表示 | B.化学巨匠及杰出贡献 |
① ② | ①张青莲--测量相对原子质量 ②侯德榜--发明联合制盐法 |
C.实验操作的先后顺序 | D.化学元素与人体健康 |
①点燃可燃性气体——先验纯后点燃 ②CO还原CuO——先加热后通入CO | ①缺铁元素--会引起贫血 ②缺碘元素--会引起甲状腺肿大 |
A.AB.BC.CD.D
【题目】Ⅰ、A、B、C、D是初中化学常见的物质,它们之间的转化关系如图所示:
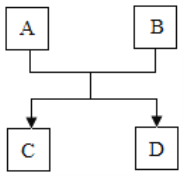
(1)若该反应为高温下进行的置换反应,且A、C为黑色固体,A具有磁性,D在常温常压下为无色无味的液体,则A的化学式为____。
(2)若该反应为A燃烧不充分的反应,且A由两种元素组成,质量比为3:1,B可供给动物呼吸,常温下C为气体,反应的化学方程式为____。
(3)若在20℃时,将B溶于乙醇中配成饱和溶液,通入适量A发生反应,且A是参与光合作用的气体,B为碱,C为纯碱,则在乙醇中该反应的化学方程式为____。20℃时,B、C在水中和乙醇中的溶解度:
物质 | 水中的溶解度 | 乙醇中的溶解度 |
B | 109g | 17.3g |
C | 21.8g | <0.01g |
Ⅱ.有一包白色粉末可能含有CuSO4、CaCl2、Na2SO4、Na2CO3、KNO3中的一种或几种,现对其进行如下实验:①取少量固体于试管中,加适量蒸馏水,固体完全溶解形成无色透明溶液;②取少量上述溶液,加过量稀硫酸,有气泡产生;③取②所得溶液少量,滴加BaCl2溶液,产生白色沉淀.分析以上实验现象,由以上实验可推断:
(1)这包白色固体中可能存在的是___;
(2)该粉末的组成有____种情况。