题目内容
【题目】化学实验室有失去标签的稀硫酸、氢氧化钠、氢氧化钙、碳酸钠、氯化钡五瓶无色溶液,现将其任意编号:A、B、C、D、E,然后两两组合进行实验,其部分现象如下表(微溶物视为可溶物):则A物质为
实验 | A+B | A+C | A+D | B+C |
现象 | 产生气体 | 产生沉淀 | 产生沉淀 | 产生沉淀 |
A.碳酸钠B.稀硫酸C.氯化钡D.氢氧化钙
【答案】A
【解析】
将五种溶液两两混合,稀硫酸和碳酸钠反应生成硫酸钠、二氧化碳和水,有气体产生,稀硫酸和氯化钡反应生成硫酸钡和盐酸,有沉淀产生,碳酸钠和氯化钡反应生成碳酸钡和氯化钠,有沉淀产生,碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,有沉淀产生,碳酸钠共产生2次沉淀,生成一次气体,可推出A为碳酸钠。
故选A。

【题目】鸡蛋主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3 , 里面覆盖一层蛋壳膜。我校兴趣小组的同学为此开展了以下探究活动:
【提出问题1】
(1)鸡蛋白中含有的营养成分是。
(2)【查阅资料】
A.蛋壳是经过自然形成。科学手段检测蛋壳中含CaCO3约82%—85%,蛋白质15%—17%,并含多种微量元素;
b.蛋壳膜中蛋白质约占90%—93%。
【提出问题2】
蛋壳中的CaCO3含量是多少呢?小华拟将该蛋壳放在空气中充分灼烧完成测定;小明拟通过蛋壳与稀盐酸反应完成测定。请你参与他们的探究。
【设计方案】他们分别称取12.0 g蛋壳设计了以下不同的实验方案:
小华的方案:
称取12.0 g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16g。则:产生的CO2质量g,蛋壳中的CaCO3的质量分数为%(结果保留到小数点后一位)。
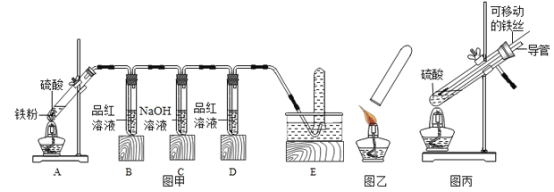
(3)小明的方案:小明设计了如下图所示的实验装置。(已知其他成分均不与稀盐酸反应,装置内试剂均足量)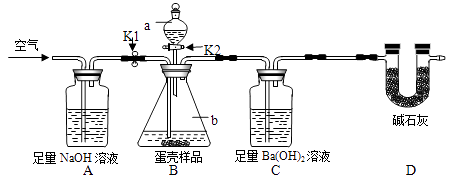
【实验步骤】
① 出编号仪器的名称:a , b;
② 按上图连接好装置后,并;
③ 向B装置中加入蛋壳样品后,先通入空气一会儿;
④ K1 , K2(填“打开”或“关闭”),向蛋壳样品中滴入10%的盐酸,直到B中为止(填实验现象);
⑤ 再通入一会儿空气,目的是;
⑥ 将装置C中的固液混合物过滤、洗涤、干燥后称量其质量;
⑦ 重复上述实验。
(4)【实验数据】重复实验,3次数据记录如下:
实验次数 | 实验1 | 实验2 | 实验3 |
装置C中沉淀质量(g) | 19.68 | 19.75 | 19.67 |
【实验分析及数据处理】
① 上述数据能否用托盘天平称量。(填“能”或“不能”)
② 若无A装置,直接通入空气,则测定结果将。(填“偏大”、“偏小”或“不变”)
③ 实验重复3次的目的是。
④ 请利用3次实验数据的平均值,计算该蛋壳中的CaCO3含量(已知:BaCO3相对分子量为197,结果保留到小数点后一位)。(请写出具体的计算过程,该空2分)
(5)【实验反思】
①下列各项措施中,能提高小明测定准确度的是(填字母序号)。
A.在装置A、B之间增加盛有浓硫酸的洗气瓶
B.缓缓滴加稀盐酸
C.在装置B、C之间增加盛有饱和NaHCO3的洗气瓶
②大家讨论后,一致认为小明的方案更合理,你认为小华方案存在较大误差的原因主要是。