题目内容
【题目】下列关于水的说法不正确的是
A.可以用肥皂水区分硬水和软水
B.对天然水进行净化的各种处理中,净化程度最高的是蒸馏
C.自然界中的水大多属于混合物
D.加明矾能使海水中的盐分沉淀而淡化
【答案】D
【解析】
试题分析:A、用肥皂水区分硬水和软水,有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水,正确,B、对天然水进行净化的各种处理中,净化程度最高的是蒸馏,得到的是蒸馏水,正确,C、自然界中的水由于含有杂质,故大多属于混合物,正确,D、加明矾溶于水形成胶状物,能吸附水的悬浮杂质,使之更快沉降,并不能能使海水中的盐分沉淀而淡化,错误,故选D

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
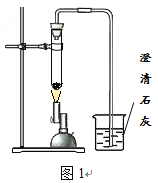
【题目】(7分)(1)小方用下图所示装置对二氧化碳的灭火实验进行研究,实验的结论是______________________________________。
(2)【提出问题】二氧化碳能否支持燃烧?
【猜想假设】镁能在二氧化碳中燃烧。
【查阅资料】①氧化镁、氢氧化镁均是白色难溶于水的固体
②![]()
③![]() ↓
↓
【实验探究】
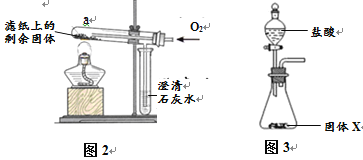
①下图中镁带剧烈燃烧,冒白烟,有黑色固体生成,并放出大量的热。
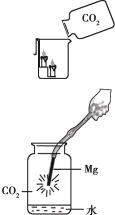
②为检验生成物的成分,做如下实验。
实验步骤 | 实验现象 | 实验结论和 化学方程式 | |
向广口瓶中加入过量盐酸,充分反应后过滤,在滤纸上留有黑色固体。 | I、将黑色固体收集、洗涤、干燥后,点燃,在火焰上方罩一个蘸有澄清石灰水的烧杯。 | 黑色固体燃烧,烧杯内壁出现白色浑浊。 | 黑色固体是 ; 涉及该步骤反应的化学方程式: 。 |
II、取少量滤液于试管中,逐滴加入氢氧化钠溶液。 | 有白色沉淀产生。 | 白烟的成分是 。 | |
③为了回收II中的白色沉淀,证明沉淀完全的实验方法是 。
(要求写出步骤、试剂、现象和结论)。
【反思提高】通过此次实验的探究,你对燃烧的条件或二氧化碳的灭火有何新认识 。