题目内容
【题目】如图流程所示,某研究小组将金属钛的冶炼(以钛铁矿为原料,其主要成分为FeTiO3)、电解食盐水和制取甲醇(CH4O)等组成产业链以提高资源的综合利用率,并减少对环境的污染。
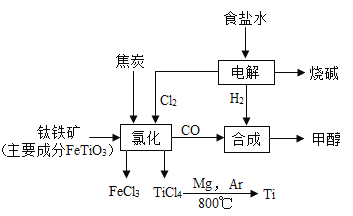
(1)绿色化学能实现“零排放”(即反应物中的原子利用率达到100%)。在一定条件下,一氧化碳与氢气反应合成甲醇就符合绿色化学的特点,则该反应的基本反应类型为_____。
(2)流程中,获得金属钛的反应原理是,在800℃和氩气(Ar)作保护气的条件下,四氯化钛(TiCl4)与镁发生置换反应生成了钛(Ti),该应的化学方程式为_____。
(3)电解时所用的食盐水是饱和的。已知20℃时NaCl的溶解度为36g,则20℃时其饱和溶液中溶质质量与溶液质量的比:m(溶质):m(溶液)是_____。为使电解过程中食盐水始终保持饱和,可采用的方法是_____。
【答案】化合反应 TiCl4+2Mg![]() 2MgCl2+Ti 9:39 增加溶质
2MgCl2+Ti 9:39 增加溶质
【解析】
(1)一氧化碳和氢气合成甲醇,该反应中两种物质反应生成一种物质,属于化合反应,故填化合反应。
(2)四氯化钛和镁在高温的条件下生成氯化镁和钛,故反应的化学方程式写为:TiCl4+2Mg![]() 2MgCl2+Ti。
2MgCl2+Ti。
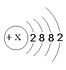
(3)20℃时NaCl的溶解度为36g,所以20℃时其饱和溶液中溶质质量与溶液质量的比:m(溶质):m(溶液)=36g:136g=9:39,故填 9:39;
为使电解过程中食盐水始终保持饱和,可采用的方法是增加溶质,故填增加溶质。

练习册系列答案
相关题目