题目内容
【题目】结合水和溶液的相关知识,回答下列问题:
![]() 对于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是______。
对于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是______。
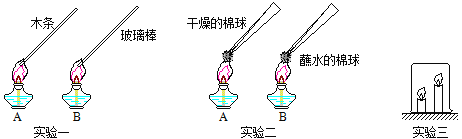
![]() 水是化学实验中常用的试剂,下列各组物质能用水鉴别的是______
水是化学实验中常用的试剂,下列各组物质能用水鉴别的是______![]() 填字母
填字母![]() 。
。
A.氢氧化钠和硝酸铵 ![]() 食盐和蔗糖
食盐和蔗糖 ![]() 高锰酸钾和碘
高锰酸钾和碘
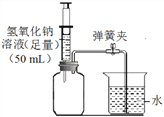
![]() 欲配制100g溶质质量分数为
欲配制100g溶质质量分数为![]() 的氯化钠溶液,完成此实验的正确操作顺序是______。
的氯化钠溶液,完成此实验的正确操作顺序是______。
![]() 溶解
溶解 ![]() 把配好的溶液装入细口瓶
把配好的溶液装入细口瓶 ![]() 称量
称量 ![]() 计算
计算 ![]() 量取
量取
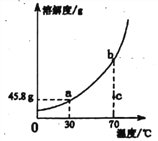
![]() 如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:
如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:
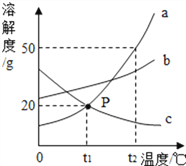
![]() 点的含义是______。
点的含义是______。
![]() 在
在![]() 时,向30克a物质中加入50克水,充分溶解后所得溶液的质量是______克。
时,向30克a物质中加入50克水,充分溶解后所得溶液的质量是______克。
![]() 将
将![]() 时a、b、c三种物质的饱和溶液升温至
时a、b、c三种物质的饱和溶液升温至![]() ,所得溶液中溶质质量分数大小关系是______。
,所得溶液中溶质质量分数大小关系是______。
![]() 物质中含有少量c物质,可用______方法提纯a物质
物质中含有少量c物质,可用______方法提纯a物质![]() 填“降温结晶”或“蒸发结晶”
填“降温结晶”或“蒸发结晶”![]() 。
。
【答案】 蒸馏 AC ![]() 在
在![]() 时,a、c的溶解度都是20g 75
时,a、c的溶解度都是20g 75 ![]() 降温结晶
降温结晶
【解析】 (1)对于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是蒸馏,蒸馏得到的水是纯水;(2)A、氢氧化钠溶于水时溶液的温度升高,硝酸铵溶于水时溶液的温度降低,用水能够鉴别;B、食盐和蔗糖溶于水无现象,不能用水鉴别;C、高猛酸钾易溶于水,碘难溶于水,用水能够鉴别;(3)欲配制100g溶质质量分数为10%的氯化钠溶液,完成此实验的正确操作顺序是:先计算需要溶质和溶剂的体积,然后称量溶质的质量、量取溶剂的体积,再进行溶解,最后把配好的溶液装入细口瓶贴上标签储存。所以顺序是:④③⑤①②;(4)①由图示可知,P点是a、c物质的溶解度曲线的交点,含义是在t1℃时,a、c的溶解度都是20g;②由a物质溶解度曲线的意义可知,在t2℃时,a物质的溶解度是50g,由溶解度的含义可知。向30克a物质中加入50克水,能溶解25g,所得溶液的质量是:50g+25=75g;③由a、b、c三种固体物质的溶解度曲线的意义可知,a、b物质的溶解度随温度的升高而增大,c物质的溶解度随温度的升高而减小,将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,a、b溶液变成了不饱和溶液,溶质的质量分数不变,c有晶体析出,由于在t1℃时b的溶解度大于a的溶解度,都大于t2℃c的溶解度,所以所得溶液中溶质质量分数大小关系是:b>a>c;④由于a物质的溶解度随温度的升高而增大,c物质的溶解度随温度的升高而减小,所以a物质中含有少量c物质,可用降温结晶方法提纯a物质。

【题目】徐州地区石灰石资源丰富。某化学兴趣小组称取4.0g石灰石样品,把40g稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入10g | 3.0g |
第二次加入10g | 2.0g |
第三次加入10g | 1.0g |
第四次加入10g | 0.6g |
请计算:
(1)4.0g石灰石样品中碳酸钙的质量是____g。
(2)10g稀盐酸能与_____g碳酸钙正好完全反应。
(3)求稀盐酸的溶质质量分数为_________(写出计算过程,结果精确到0.1%)