题目内容
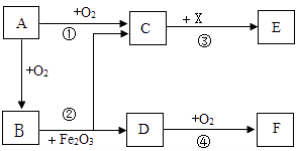
【题目】回收利用废金属可减少资源浪费、保护环境.某工厂利用含铜废料(含Cu、Zn及不溶于水、不参加下列反应的其他杂质)制取铜并得到硫酸锌溶液,主要流程如下: 
己知:2Cu+2H2SO4+O2═2CuSO4+2H2O
(1)操作①生成气体的反应属于反应类型(填“化合”、“分解”、“置换”);
(2)操作②的名称是 , 在该流程中操作②过程必须禁止明火,其原因是:(用化学方程式表示);
(3)在整个流程中重新生成铜的化学方程式为 .
【答案】
(1)置换
(2)过滤;2H2+O2 ![]() 2H2O
2H2O
(3)Zn+CuSO4═ZnSO4+Cu
【解析】解:(1)操作①生成气体的过程中,锌和稀硫酸反应生成硫酸锌和氢气,属于置换反应.故填:置换.(2)操作②的名称是过滤,在该流程中操作②过程必须禁止明火,其原因是氢气和空气或氧气混合达到爆炸极限时,遇明火会发生爆炸,反应的化学方程式为:2H2+O2 ![]() 2H2O.
2H2O.
故填:过滤;2H2+O2 ![]() 2H2O.(3)在整个流程中,锌能和硫酸铜反应生成硫酸锌和铜,反应的化学方程式为:Zn+CuSO4═ZnSO4+Cu.
2H2O.(3)在整个流程中,锌能和硫酸铜反应生成硫酸锌和铜,反应的化学方程式为:Zn+CuSO4═ZnSO4+Cu.
故填:Zn+CuSO4═ZnSO4+Cu.
【考点精析】利用书写化学方程式、文字表达式、电离方程式对题目进行判断即可得到答案,需要熟知注意:a、配平 b、条件 c、箭号.

【题目】秸秆是农村的常见品,平均含硫量达千分之三点八(3.8‰),燃料后,其中的硫元素转化为SO2引起空气污染.假设我国空气质量标准对空气中二氧化硫的浓度级别规定如表所示(空气中二氧化硫的浓度用单位体积的空气中所含二氧化硫的质量表示).
浓度级别 | 标准(mg/m3) |
一级 | 浓度≤0.15 |
二级 | 0.15<浓度≤0.50 |
三级 | 0.50<浓度≤0.70 |
若某4m3空气恰好能与含碘(I2)5.08mg的碘水完全反应(该反应的化学方程式是:SO2+I2+2H2O=H2SO4+2HI),试通过计算说明此空气中二氧化硫的浓度级别.