题目内容
【题目】(5分)氧(O)是海水中含量最多的元素,根据下图信息回答下列问题:
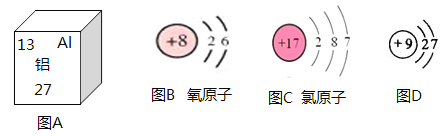
(1)图A表示的原子核电荷数为__________;
(2)在地壳中,按____________计算(填“体积分数”或“质量分数”),氧元素含量接近50%;
(3)图B表示的原子在化学变化中形成的离子符号为_________
(4)图D表示的是___________(填“金属”或“非金属”或“稀有气体”)元素的原子,其化学性质与图________表示的原子的化学性质相似(填字母序号)
【答案】(1)13 (2)质量分数 (3)O2- (4)非金属 图C
【解析】
试题分析:(1)图A表示的原子的原子序数为13,而原子序数=核电荷数为13
(2)在地壳中,按质量分数计算,氧元素含量接近50%
(3)图B表示的原子,它的最外层电子数为6﹥4,容易得到2个电子,带上2个单位的负电荷,成为阴离子,故在化学变化中形成的离子符号为:O2-
(4)图D的最外层电子数为7﹥4,表示的是非金属元素的原子,化学性质与最外层电子数关系密切,最外层电子数相等,化学性质相似,故其化学性质与图C表示的原子的化学性质相似,最外层电子数都为7

 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】(14分)利用下列所示仪器、药品(及其它必要物品)设计制取氧气和试验其性质的实验对比方案。
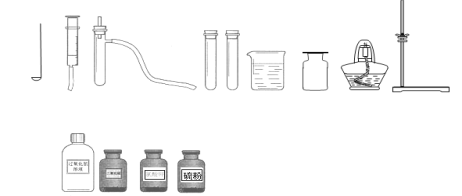
(1)对比加入试剂顺序对于制取氧气反应速率的影响
方法一:把二氧化锰加入装有过氧化氢溶液的试管中
| 方法二:把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中
|
现象:方法一中,立即产生大量的气泡,一会儿,产生气泡的速度越来越慢; 方法二中,持续并均匀地产生气泡; | |
结论:方法__①____可以得到平稳的氧气流。通过对比实验可知,对于固体和液体反应制取气体时,加入试剂的顺序对反应速率有影响,若想得到平稳的气流,应该先加___②____,(填“固体”或“液体”,下同)然后再缓缓加入 _____③_____ | |
(2)对比不同反应物制取氧气的反应速率
反应物药品的名称 | 反应的文字表达式 | 填选用制取和收集装置的仪器名称 |
方法一:过氧化氢溶液、二氧化锰 | ①_____________________ | 试管(带支管)、注射器、__②____ |
方法二:氯酸钾、二氧化锰 | ③___________________ | 此空不用填 |
结论:对比两种制取氧气的方法,方法一更简单。因为同样在二氧化锰的催化剂下,该方法制取氧气反应迅速,______ ④ _________。 | ||
(3)对比硫在空气里与在氧气中燃烧的现象
实验名称 | 操作步骤 | 实验现象 |
硫在空气里燃烧 | 取少量的硫粉于燃烧匙中,把燃烧匙放置在外焰上加热至硫粉燃烧起来,观察现象 | ①_____________________ |
硫在氧气中燃烧 | ②_____________________ | 在氧气中燃烧更剧烈,发出_____③____火焰,放热,生成有刺激性气味的气体 |
结论:条件(如浓度、温度)对化学反应是有影响的。硫在空气中燃烧不如在氧气中燃烧剧烈,是因为空气中_________④_________相对较少。 | ||

