题目内容
【题目】如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题: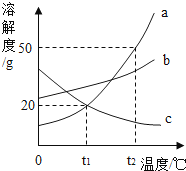
(1)若使a、c的饱和溶液同时析出晶体,方法是 .
(2)℃时,a、c两物质的溶解度相等.气体的溶解度随温度的变化规律与(填“a”、“b”或“c”)相似.
(3)在t2℃时,a、b、c三种饱和溶液降温至t1℃时溶质的质量分数由大到小的顺序是 , 析出晶体最多的是(填“a”、“b”或“无法确定”).
(4)在t2℃时,将150克a的饱和溶液稀释成质量分数为20%的溶液需加水克.
【答案】
(1)蒸发溶剂
(2)t1;c
(3)b>a>c;无法确定
(4)100
【解析】解:(1)a的溶解度随着温度的升高而增大,c的溶解度随着温度的升高而减小,因此若使a、c的饱和溶液同时析出晶体,方法是蒸发溶剂;(2)t1℃时,a、c两物质的溶解度相等;气体的溶解度随温度的变化规律与c相似;(3)在t2℃时,b的溶解度大于a的溶解度,因此b的质量分数大于a的质量分数,由于a在t1℃时的溶解度大于c在t2℃时的溶解度,因此a的质量分数大于c的质量分数,a、b、c三种饱和溶液降温至t1℃时溶质的质量分数由大到小的顺序是b>a>c;因为不知道饱和溶液的质量,因此无法确定析出晶体的多少;(4)设加入水的质量为x,在t2℃时,a的溶解度是50g,150克a的饱和溶液中含有50g溶质a,因此有:50g=(150g+x)×20%,
x=100g.故填:蒸发溶剂;t1;c;b>a>c;无法确定;100.
【考点精析】本题主要考查了固体溶解度曲线及其作用和气体溶解度的影响因素的相关知识点,需要掌握1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和);气体的溶解度:(1)气体溶解度的定义:在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积.(2)影响因素: ①气体的性质②温度(温度越高,气体溶解度越小)③压强(压强越大,气体溶解度越大)才能正确解答此题.

【题目】水和溶液在生命活动和生产、生活中起着十分重要的作用,请回答下列问题:
(1)在水的净化过程中,常利用(填物质名称)的吸附性除去水中异味,净化过的水通入氯气后输送到每家每户,其中通入氯气的作用是 .
(2)如表是NaOH和Ca(OH)2的溶解度数据(单位:g/100g水),请回答下列问题.
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 | NaOH | 31 | 90 | 111 | X | 313 | 336 |
Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
Ⅰ.表示溶解度的符号是;表中“111”数字表示的含义是 .
Ⅱ.为测定X的值,取4份60℃的水各50克,分别进行实验,并记录数据如表:
试验编号 | 实验1 | 实验2 | 实验3 | 实验4 |
NaOH质量/g | 50 | 60 | 70 | 50 |
H2O质量/g | 50 | 50 | 50 | 50 |
溶液质量/g | 100 | 110 | 114.5 | 114.5 |
(3)【实验结果分析】实验1所得溶液的质量分数为;由实验可知X的值为 .
Ⅲ.除去NaOH溶液中混有的少量Ca(OH)2 , 通过蒸发浓缩、 , 然后过滤、洗涤、干燥得到NaOH固体.
Ⅳ.现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后,恢复到原来温度得到的溶液(乙溶液),甲、乙溶液中溶质质量甲乙(填“>、<、=”).
Ⅴ.在20℃时,向盛有100g水的烧杯中加入111gNaOH,欲使其完全溶解变成不饱和溶液,下列说法中正确的是 .
a、溶液的质量可能不变 b、溶质的质量分数一定减小
c、溶液中溶质的质量一定增大 d、可以升温到40℃以上
e、NaOH的溶解度一定变大 f、20℃时加入的水的质量>23.4g.