题目内容
【题目】钛和钛合金被认为是21世纪重要的金属材料,钛合金与人体具有很好的“相容性”,可用于制造人造骨骼,工业上以钛铁矿(主要成分为钛酸亚铁,FeTiO3)为原料生产钛,其工业流程示意图如下: 请回答: 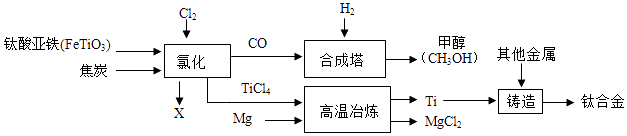
(1)钛合金属于(选填“混合物”、“纯净物”).
(2)钛酸亚铁FeTiO3中钛的化合价为价.
(3)以CO与H2在合成塔中生产甲醇(CH3OH)属于化合反应,其化学方程式为
(4)经高温冶炼得到金属钛,则参加反应的镁与钛的质量比为 .
(5)氯化过程中主要发生的反应为2FeTiO3+6C+7Cl2 ![]() 2TiCl4+2X+6CO,则X的化学式为 .
2TiCl4+2X+6CO,则X的化学式为 .
【答案】
(1)混合物
(2)+4
(3)CO+2H2 ![]() CH3OH
CH3OH
(4)1:1
(5)FeCl3
【解析】解:(1)钛合金属于混合物. 故填:混合物.(2)设钛酸亚铁中钛的化合价为x,
其中铁元素化合价是+2,氧元素化合价是﹣2,根据题意有:(+2)+x+(﹣2)×3=0,
x=+4,
故填:+4.(3)以CO与H2在合成塔中生产甲醇(CH3OH)属于化合反应,其化学方程式为:CO+2H2 ![]() CH3OH.
CH3OH.
故填:CO+2H2 ![]() CH3OH.(4)四氯化钛和镁反应的化学方程式及其质量关系为:
CH3OH.(4)四氯化钛和镁反应的化学方程式及其质量关系为:
TiCl4+ | 2Mg | Ti |
48 | 48 |
则参加反应的镁与钛的质量比为:48:48=1:1.
故填:1:1.(5)由2FeTiO3+6C+7Cl2 ![]() 2TiCl4+2X+6CO可知,反应前后钛原子都是2个,氧原子都是6个,碳原子都是6个,反应前铁原子是2个,反应后应该是2个,包含在2X中,反应前氯原子是14个,反应后应该是14个,其中6个包含在2X中,则X的化学式为.
2TiCl4+2X+6CO可知,反应前后钛原子都是2个,氧原子都是6个,碳原子都是6个,反应前铁原子是2个,反应后应该是2个,包含在2X中,反应前氯原子是14个,反应后应该是14个,其中6个包含在2X中,则X的化学式为.
故填:FeCl3 .
【考点精析】解答此题的关键在于理解质量守恒定律及其应用的相关知识,掌握①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏,以及对书写化学方程式、文字表达式、电离方程式的理解,了解注意:a、配平 b、条件 c、箭号.

【题目】化学反应速率是衡量化学反应进行快慢的物理量,为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验. 三个小组均可采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的H2O2溶液、MnO2、CuO、红砖粉末.
A组:探究催化剂对化学反应速率的影响
取5mL10%H2O2溶液,三次实验分别加入0.5gMnO2、红砖粉末、CuO进行实验,记录数据如下:
试剂 | MnO2 | 红砖粉末 | CuO |
t/s | 10 | 60 | 20 |
由此可出结论:MnO2、CuO对H2O2分解有催化作用,红砖粉末无催化作用,某同学对该结论提出疑问.
补充对比实验,操作为 .
结果:长时间(大于100s),收集到很少量气体.
更正结论:红砖粉末(选填“有”、“无”)催化作用,三者中催化效率最高.
B组:探究浓度对化学反应速率的影响
甲同学:取10mL5%H2O2溶液,加入0.5gMnO2为催化剂,进行实验,记录时间t1 .
乙同学:取10mL2.5%H2O2溶液,加入0.5gMnO2为催化剂,进行实验,记录时间t2 .
实验结果 .
结论:浓度越大,反应速率越快.
丙同学:对实验设计提出疑问,并补充实验 .
记录时间t3 , 且t1<t3<t2 .
更正结论为:当时,反应物浓度越大,反应速率越快.
C组:探究对化学反应速率的影响.
取10mL5%H2O2溶液和0.5gCuO为催化剂进行实验,两次实验分别将试管置于冰水浴和50℃热水浴记录时间t4、t5 , 且t4>t5 .
结论:当反应物浓度和催化剂相同时, .
综上所述:①为了研究某一因素对化学反应速率的影响,必须 .
②探究发现影响化学反应速率的因素有 .