题目内容
 某同学发现他家菜园中的蔬菜生长迟缓,便施用了一种含氮的化学肥料,下图是该氮肥包装标签上的部分文字,请仔细阅读回答下列问题:
某同学发现他家菜园中的蔬菜生长迟缓,便施用了一种含氮的化学肥料,下图是该氮肥包装标签上的部分文字,请仔细阅读回答下列问题:(1)硝酸铵是由
3
3
种元素组成;(2)硝酸铵的相对分子质量
80
80
;(3)这袋氮肥中氮元素的质量为
17.15kg
17.15kg
;(4)该氮肥中硝酸铵的质量分数为多少?(写出计算过程,结果保留一位小数)
分析:(1)根据硝酸铵化学式的含义进行分析解答.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据题意,一袋化肥的质量为50kg,含氮量为34.3%,据此进行分析解答.
(4)样品中尿素的质量分数(纯度)可理解为:
×100%,根据此公式进行计算即可.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(3)根据题意,一袋化肥的质量为50kg,含氮量为34.3%,据此进行分析解答.
(4)样品中尿素的质量分数(纯度)可理解为:
| 化肥中氮元素的质量分数 |
| 纯净的硝酸铵中氮元素的质量分数 |
解答:解:(1)硝酸铵是由氮、氢、氧三种元素组成的.
(2)硝酸铵的相对分子质量为14×2+1×4+16×3=80.
(3)由题意,一袋化肥的质量为50kg,含氮量为34.3%,则含氮元素的质量为:50kg×34.3%=17.15kg.
(4)根据化合物中元素的质量分数=
×100%,硝酸铵中氮元素的质量分数是
×100%=35%,
该氮肥中硝酸铵的质量分数为=
×100%=98%.
故答案为:(1)3;(2)80;(3)17.15kg;(4)98%.
(2)硝酸铵的相对分子质量为14×2+1×4+16×3=80.
(3)由题意,一袋化肥的质量为50kg,含氮量为34.3%,则含氮元素的质量为:50kg×34.3%=17.15kg.
(4)根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
| 14×2 |
| 80 |
该氮肥中硝酸铵的质量分数为=
| 34.3% |
| 35% |
故答案为:(1)3;(2)80;(3)17.15kg;(4)98%.
点评:本题难度不大,考查同学们结合标签新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某同学发现他家菜园中的蔬菜生长迟缓,便施用了一种含有硝酸铵的氮肥,含氮量为30%,加入此化肥中只含一种杂质,则此种氮肥中不可能混入的一种杂质为( )
| A、氯化铵 | B、碳铵 | C、尿素 | D、硫酸铵 |
 某同学发现他家菜园中的蔬菜生长迟缓,便购买施用了一包化肥,右图为该包化肥的外包装标签上的部分说明,请仔细阅读标签并回答下列问题(纯度--化肥中硝酸铵的质量分数):
某同学发现他家菜园中的蔬菜生长迟缓,便购买施用了一包化肥,右图为该包化肥的外包装标签上的部分说明,请仔细阅读标签并回答下列问题(纯度--化肥中硝酸铵的质量分数):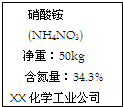 某同学发现他家菜园中的蔬菜生长迟缓,便施用了一种氮肥,右图是氮肥包装标签上的部分文字.请回答:该肥料的实际纯度是多少?
某同学发现他家菜园中的蔬菜生长迟缓,便施用了一种氮肥,右图是氮肥包装标签上的部分文字.请回答:该肥料的实际纯度是多少? 某同学发现他家菜园中的蔬菜生长迟缓,便购买施用了一包化肥,右图为该包化肥的外包装标签上的部分说明,请仔细阅读标签并回答下列问题(纯度--化肥中硝酸铵的质量分数):
某同学发现他家菜园中的蔬菜生长迟缓,便购买施用了一包化肥,右图为该包化肥的外包装标签上的部分说明,请仔细阅读标签并回答下列问题(纯度--化肥中硝酸铵的质量分数):