题目内容
下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明.请根据此表,结合所学知识,回答下列问题.| 配料表 | 精制海盐,碘酸钾 |
| 含碘量/kg | 20g~40g |
| 包装日期 | 见封底 |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
(2)根据加碘食盐的储藏方法和食用方法可推测:碘酸钾的化学性质 (填“稳定”或“不稳定”).
(3)从2000年10月1日起.我国食盐中加碘含量将调整为每千克食盐中含碘约为0.035g,相当于每千克食盐中含碘酸钾 g.
【答案】分析:(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进行分析解答;化合物中元素的质量分数 ×100%,进行分析解答;根据在化合物中正负化合价代数和为零,结合碘酸钾(KIO3)的化学式计算化合价;
×100%,进行分析解答;根据在化合物中正负化合价代数和为零,结合碘酸钾(KIO3)的化学式计算化合价;
(2)烹调时待食品熟后再加入碘盐,说明碘盐的热稳定性差,受热容易分解;
(3)根据化合物的质量=化合物中某元素的质量÷该元素在化合物中的质量分数进行分析.
解答:解:(1)碘酸钾(KIO3)的相对分子质量=39+127+16×3=214.
碘酸钾(KIO3)中碘元素的质量分数=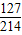 ×100%=59.3%.
×100%=59.3%.
钾元素显+1,氧元素显-2,设碘元素的化合价是x,根据在化合物中正负化合价代数和为零,可知碘酸钾(KIO3)中碘元素的化合价:(+1)+x+(-2)×3=0,则x=+5.
故答案为:214;59.3%;+5;
(2)由食用方法说明可知,碘酸钾在受热时易分解,热稳定性差,故答案为:不稳定;
(3)每千克食盐含碘0.035克,相当于每千克食盐含碘酸钾的质量=0.035g÷59.3%=0.059g,故答案为:0.059.
点评:本题难度不大,考查学生利用化合价的原则、灵活运用化学式的有关计算进行分析问题、解决问题的能力,同时要善于从说明中总结物质的性质.
 ×100%,进行分析解答;根据在化合物中正负化合价代数和为零,结合碘酸钾(KIO3)的化学式计算化合价;
×100%,进行分析解答;根据在化合物中正负化合价代数和为零,结合碘酸钾(KIO3)的化学式计算化合价;(2)烹调时待食品熟后再加入碘盐,说明碘盐的热稳定性差,受热容易分解;
(3)根据化合物的质量=化合物中某元素的质量÷该元素在化合物中的质量分数进行分析.
解答:解:(1)碘酸钾(KIO3)的相对分子质量=39+127+16×3=214.
碘酸钾(KIO3)中碘元素的质量分数=
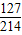 ×100%=59.3%.
×100%=59.3%.钾元素显+1,氧元素显-2,设碘元素的化合价是x,根据在化合物中正负化合价代数和为零,可知碘酸钾(KIO3)中碘元素的化合价:(+1)+x+(-2)×3=0,则x=+5.
故答案为:214;59.3%;+5;
(2)由食用方法说明可知,碘酸钾在受热时易分解,热稳定性差,故答案为:不稳定;
(3)每千克食盐含碘0.035克,相当于每千克食盐含碘酸钾的质量=0.035g÷59.3%=0.059g,故答案为:0.059.
点评:本题难度不大,考查学生利用化合价的原则、灵活运用化学式的有关计算进行分析问题、解决问题的能力,同时要善于从说明中总结物质的性质.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明.请根据此表,结合所学知识,回答下列问题.
| 配料表 | 精制海盐,碘酸钾 |
| 含碘量/kg | 20g~40g |
| 包装日期 | 见封底 |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
(2)根据加碘食盐的储藏方法和食用方法可推测:碘酸钾的化学性质______(填“稳定”或“不稳定”).
(3)从2000年10月1日起.我国食盐中加碘含量将调整为每千克食盐中含碘约为0.035g,相当于每千克食盐中含碘酸钾______g.
下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明.请根据此表,结合所学知识,回答下列问题.
(1)碘酸钾的化学式为KIO3,则碘酸钾的相对分子质量为 ,其中碘元素的质量分数为 ,碘元素的化合价为 价.
(2)根据加碘食盐的储藏方法和食用方法可推测:碘酸钾的化学性质 (填“稳定”或“不稳定”).
(3)从2000年10月1日起.我国食盐中加碘含量将调整为每千克食盐中含碘约为0.035g,相当于每千克食盐中含碘酸钾 g.
| 配料表 | 精制海盐,碘酸钾 |
| 含碘量/kg | 20g~40g |
| 包装日期 | 见封底 |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
(2)根据加碘食盐的储藏方法和食用方法可推测:碘酸钾的化学性质 (填“稳定”或“不稳定”).
(3)从2000年10月1日起.我国食盐中加碘含量将调整为每千克食盐中含碘约为0.035g,相当于每千克食盐中含碘酸钾 g.
