题目内容
甲、乙、丙三种固体物质的溶解度曲线如右图所示,由图可知: 物质的溶解度随温度升高而减小; t1℃时 物质的溶解度最大;t2℃时,甲、乙两种饱和溶液溶质的质量分数 (填 “相等”、“不相等”、 “不一定”);当甲中含有少量乙时,可以用 法(填“降温结晶”、“蒸发结晶”、“过滤”)提纯甲。

(4分)丙 乙 相等 降温结晶
分析:根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度的大小,②判断某物质的溶解度随温度变化的变化情况,③判断采取降温还是蒸发溶剂的方法达到提纯物质的目的等,注意同温度下的某物质的溶解度和其饱和溶液中溶质的质量分数间的关系:饱和溶液中溶质的质量分数=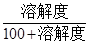 ×100%,因此溶解度大,则饱和溶液中溶质的质量分数就大.
×100%,因此溶解度大,则饱和溶液中溶质的质量分数就大.
解答:解:(1)从三物质的溶解度曲线可以看出,甲和乙的溶解度都随温度的升高而增大,丙的溶解度随温度的升高而减小,故答案为:丙.
(2)有三物质的溶解度曲线不难看出,在t1℃时,乙的溶解度最大,故答案为:乙.
(3)在t2℃时,甲和乙的溶解度相等,因此它们的饱和溶液中溶质的质量分数相等,故答案为:相等.
(4)由于甲和乙的溶解度都随温度的升高而增大,但甲的溶解度受温度的影响很大,而乙的溶解度受温度的影响小,因此提纯混有少量乙的甲时,应采取降温结晶的方法,故答案为:降温结晶.
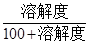 ×100%,因此溶解度大,则饱和溶液中溶质的质量分数就大.
×100%,因此溶解度大,则饱和溶液中溶质的质量分数就大.解答:解:(1)从三物质的溶解度曲线可以看出,甲和乙的溶解度都随温度的升高而增大,丙的溶解度随温度的升高而减小,故答案为:丙.
(2)有三物质的溶解度曲线不难看出,在t1℃时,乙的溶解度最大,故答案为:乙.
(3)在t2℃时,甲和乙的溶解度相等,因此它们的饱和溶液中溶质的质量分数相等,故答案为:相等.
(4)由于甲和乙的溶解度都随温度的升高而增大,但甲的溶解度受温度的影响很大,而乙的溶解度受温度的影响小,因此提纯混有少量乙的甲时,应采取降温结晶的方法,故答案为:降温结晶.

练习册系列答案
相关题目







