题目内容
【题目】下面是实验室常用仪器组成的装置,请回答下列问题:
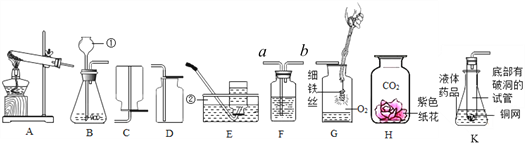
(1)指出标号仪器的名称:①________②__________;
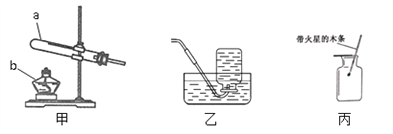
(2)用氯酸钾制取氧气的化学方程式为__________;基本反应类型是_________;实验室制取二氧化碳的反应方程式是________;若用F装置进行排空气发收集CO2,CO2从F装置的_____(填“a”或“b”)导管口通入;
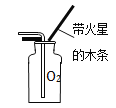
(3)已知氨气是一种极易溶于水的气体,密度比空气小,实验室可用氧化钙固体与浓氨水在常温下混合制成氨气(NH3),则应选用的气体发生装置是_________(填装置序号),收集装置是________(填装置序号)。用收集到的氧气完成如G图所示实验,G中发生反应的化学方程式是_________,G中瓶底要放少量水的目的是____________。
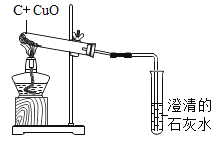
﹙4﹚K图是某同学利用底部有破洞的试管设计的制二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点:___________。若将铜网改成铁网,产生的后果之一是收集到的气体不纯,原因是(用化学方程式表示)____________。
【答案】长颈漏斗 水槽 2KClO3![]() 2KCl+3O2 分解反应 CaCO3+2HClCaCl2+2H2O+CO2↑ b端 B C 3Fe+2O2
2KCl+3O2 分解反应 CaCO3+2HClCaCl2+2H2O+CO2↑ b端 B C 3Fe+2O2![]() Fe3O4 防止高温熔融物使瓶底炸裂 控制反应的发生与停止 Fe+2HCl2FeCl2+H2↑
Fe3O4 防止高温熔融物使瓶底炸裂 控制反应的发生与停止 Fe+2HCl2FeCl2+H2↑
【解析】
本题主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、检查装置的气密性、注意事项和有关化学方程式的书写等,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。
(1)标号仪器的名称分别为;长颈漏斗、水槽 ;
(2)氯酸钾制取氧气时生成了氯化钾和氧气,化学方程式为2KClO3![]() 2KCl+3O2↑,该反应是一种物质生成两种物质,属于分解反应;实验室制取二氧化碳是用碳酸钙和盐酸反应生成二氧化碳和氯化钙和水,反应方程式是CaCO3+2HClCaCl2+2H2O+CO2↑;二氧化碳的密度大于空气,若用F装置进行排空气发收集CO2,CO2从F装置的 b导管口通入;
2KCl+3O2↑,该反应是一种物质生成两种物质,属于分解反应;实验室制取二氧化碳是用碳酸钙和盐酸反应生成二氧化碳和氯化钙和水,反应方程式是CaCO3+2HClCaCl2+2H2O+CO2↑;二氧化碳的密度大于空气,若用F装置进行排空气发收集CO2,CO2从F装置的 b导管口通入;
(3)氧化钙是固态的,氨水是液态的,该反应在常温下进行,属于固—液常温型,应选用的气体发生装置是B;氨气是一种极易溶于水的气体,密度比空气小气体,所以不能用排水法收集,只能用向下排空气法收集,应选用收集装置是C;铁和氧气在点燃的条件下生成四氧化三铁,反应的化学方程式是3Fe+2O2![]() Fe3O4;铁丝在氧气中燃烧放出大量的热,集气瓶G底部盛有少量水或细沙的原因是:防止高温熔融物使瓶底炸裂。
Fe3O4;铁丝在氧气中燃烧放出大量的热,集气瓶G底部盛有少量水或细沙的原因是:防止高温熔融物使瓶底炸裂。
(4)通过控制试管在锥形瓶内的位置,可以实现固体和液体的分离,所以除了废物利用的优点外,另一个优点是:控制反应的发生与停止,铁能与盐酸反应生成氯化亚铁和氢气,若将铜网改成铁网,产生的后果之一是收集到的气体不纯,原因是(用化学方程式表示) Fe+2HCl2FeCl2+H2↑。

 阅读快车系列答案
阅读快车系列答案