题目内容
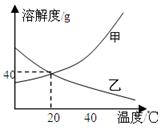
(7分,第1空1分其余每空2分)甲、乙两物质的溶解度曲线如图所示,请据图回答下列问题。
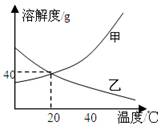
(1)20℃时,甲物质的溶解度是 g;
(2)20℃时,甲物质的饱和溶液中溶质和溶剂的质量比为 ;
(3)欲将40℃时乙物质的饱和溶液变为不饱和溶液,可采用的方法是 ;(写一种即可)
(4)40℃时,将甲、乙两物质的饱和溶液分别降温到20℃,所得溶液的溶质质量分数的大小关系是 。
【答案】
(1)40(1分) (2)2︰5 (3)加水或降温 (4)甲大于乙
【解析】:(1)根据甲的溶解度曲线可知,在20℃时,甲的溶解度是40g,故答案为:40 (2)由于甲在20℃时甲的溶解度是40g,即100g水中最多溶解甲物质40g形成140g饱和溶液,则在20℃时,甲的饱和溶液中溶质和溶剂的质量比为40:100=2:5,故答案为:2:5
(3)由于乙的溶解度随温度的升高而减小,因此若把它的饱和溶液变为不饱和溶液,可以采取降低温度或增加溶剂的方法,故答案为:降低温度
(4)40℃时,将甲、乙两物质的溶解度甲大于乙,所以该温度下甲乙的饱和溶液溶质质量分数也是甲大于乙;降低温度甲的溶解度减小析出晶体,溶质质量分数减小,乙的溶解度增大,但不会析出晶体所以溶液的溶质质量分数不变;降温到20℃甲仍是饱和溶液,溶质质量分数=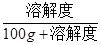 ×100%,温度从40℃降温到20℃时乙不饱和,溶质质量分数小于
×100%,温度从40℃降温到20℃时乙不饱和,溶质质量分数小于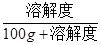 ×100%,20℃时甲乙的溶解度相等,所以得出该温度时所得溶液溶质质量分数甲大于乙,故答案:甲>乙
×100%,20℃时甲乙的溶解度相等,所以得出该温度时所得溶液溶质质量分数甲大于乙,故答案:甲>乙

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目