题目内容
 溶液在生产和生活中有重要意义.
溶液在生产和生活中有重要意义.(1)碘酒溶液中溶剂是
(2)用含有洗涤剂的水可以将餐具上的油滴清洗干净的原因是
①油滴可以溶解于水②洗涤剂有乳化功能③洗涤剂有吸附作用
(3)配制500g 0.8%的食盐水需要称量食盐
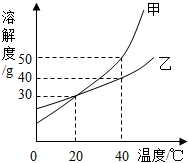
(4)甲、乙两种固体的溶解度曲线如右图所示.回答下列相关问题:
①通过右图可知:20℃甲的溶解度
②40℃时,在100g水中加入50g甲,所得溶液的质量是
分析:弄清固体溶解度的概念(在一定温度下,某固体物质在100克水中达到饱和状态时所溶解的质量)、固体溶解度曲线所表示的意义及饱和溶液中溶质的质量分数和同温度下的溶解度之间的关系.
解答:解:(1)碘酒指的是碘的酒精溶液,石灰水是氢氧化钙的溶液,故答案为:酒精,氢氧化钙
(2)洗涤剂能去油污,主要是利用乳化作用,故答案为:②
(3)溶质的质量═溶液的质量×溶质的质量分数,故需食盐的质量为:500g×0.8%═4g,故答案为:4
(4)①观察两物质的溶解度曲线可知,在20℃时两物质的溶解度曲线相交于一点,即在20℃时两物质的溶解度相等,故答案为:等于
②由于在40℃时,甲的溶解度是50克,即在100克水中最多溶解50克甲,因此在100g水中加入50g甲,会形成150克饱和溶液,若将该饱和溶液降温至20℃时,由于在20℃时甲的溶解度只有30克,因此会析出晶体20克,则剩余溶液中溶质的质量分数是
×100%═23.1%,故答案为:150,23.1%
(2)洗涤剂能去油污,主要是利用乳化作用,故答案为:②
(3)溶质的质量═溶液的质量×溶质的质量分数,故需食盐的质量为:500g×0.8%═4g,故答案为:4
(4)①观察两物质的溶解度曲线可知,在20℃时两物质的溶解度曲线相交于一点,即在20℃时两物质的溶解度相等,故答案为:等于
②由于在40℃时,甲的溶解度是50克,即在100克水中最多溶解50克甲,因此在100g水中加入50g甲,会形成150克饱和溶液,若将该饱和溶液降温至20℃时,由于在20℃时甲的溶解度只有30克,因此会析出晶体20克,则剩余溶液中溶质的质量分数是
| 30 |
| 100+30 |
点评:主要考查了对固体溶解度概念的理解及固体的溶解度曲线的意义,培养学生的理解能力、分析能力和应用知识的能力.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
 28、 溶液在生产和生活中有重要意义.
28、 溶液在生产和生活中有重要意义.

 (2009?西宁)溶液在生产和生活中有重要意义.
(2009?西宁)溶液在生产和生活中有重要意义.