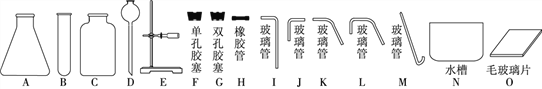
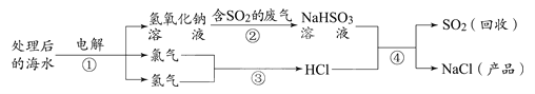
题目内容
【题目】下表为元素周期表的部分示意图,表中数字为各元素原子的质子数,利用下表回答相关问题。
1 H | 2 He | ||||||||||||||||
3 Li | 4 Be | 5 B | 6 C | 7 N | 8 O | 9 F | 10 Ne | ||||||||||
11 Na | 12 Mg | 13 Al | 14 Si | 15 P | 16 S | 17 Cl | 18 Ar | ||||||||||
① | ② | ③ |
(1)写出带一个单位负电荷且核内质子数为17的离子_____;
(2)研究表中各元素原子的质子数,可发现元素从左到右的排列规律是_____________;
(3)请预测质子数为19的元素在表中的位置________(填①、②、③)。该元素对应离子的结构示意图为______________。
【答案】 Cl- 同一周期的元素从左向右的质子数依次增大(符合题意即可 ) ① ![]()
【解析】本题考查了元素周期表的特点及其应用,离子结构示意图的书写。
(1) 核内质子数为17是氯元素,带一个单位负电荷且核内质子数为17的离子符号是Cl-;
(2)研究表中各元素原子的质子数,可发现元素从左到右的排列规律是同一周期的元素从左向右的质子数依次增大;
(3)质子数为19的元素的原子核外电子排布是2、8、8、1,最外层电子数是1,与钠原子的最外层电子数相同,应排在钠元素的下方,在表中的位置①;该元素的原子在化学变化中易失去1个电子,该元素对应离子的结构示意图为![]() 。
。

 走进文言文系列答案
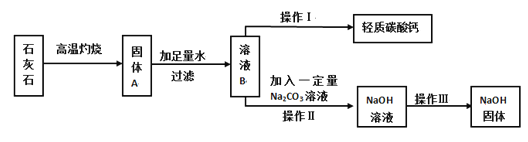
走进文言文系列答案【题目】某草木灰(主要成分为K2CO3,杂质不溶于水)样品,可能还添加了K2SO4、KCl。某化学兴趣小组进行了如下实验:
(1)样品的预处理:

①操作a的名称为__________________,其目的是____________________
②溶液A中主要的阴离子,除CO32-外,可能还含有_______________(填离子符号)
(2)样品成分的确定:设计实验方案,完成下述表格;限选试剂:稀盐酸、稀硝酸、稀硫酸、氯化钡溶液、硝酸钡溶液、硝酸银溶液
实验操作 | 预期现象和必要结论 |
步骤1:取溶液A少量于试管中,加入足量 _______________,充分振荡,静置,过滤。 |
|
步骤2:取少量步骤1所得的滤液于试管中,____________ | ______,说明样品中未添加KCl |
步骤3:取少量步骤1所得的滤渣于试管中,__________________ | ______,说明样品中添加了K2SO4 |