题目内容
【题目】水在自然界净化中要把有机污物自发地转变为简单的无机物质时,需要水中含有一定的氧气[有机物(C、H、O)+O2→CO2+H2O],1 L水中含有的有机物转变为无机物所需要的氧的量称为生化需氧量(BOD),用g/L为单位表示,如果水的氧气量比BOD少,水就发臭,鱼和其他淡水生物就不会生存.某地区一条河水里有机物的质量分数为0.001%,此有机物的化学式可用C6H10O5表示,已知在正常大气压条件下,氧气在水中的溶解量是0.092 g/L.
(1)写出有机物在有氧气条件下转化为无机物的化学方程式
(2)这条河水的生化需氧量为 .
(3)这条河中的鱼类 (填“能”“不能”)维持生命.
【答案】(1)C6H10O5+6O2![]() 6CO2+5H2O;(2)0.01185g/L;(3)不能.
6CO2+5H2O;(2)0.01185g/L;(3)不能.
【解析】(1)C6H10O5与氧气反应生成二氧化碳和水.
该反应的化学方程式为:C6H10O5+6O2![]() 6CO2+5H2O.
6CO2+5H2O.
(2)1L河水的质量为:1000g/L×1L=1000g
1L河水中有机物的质量为:1000g×0.001%=0.01g
设转化1g有机物需要氧气的质量为x.
C6H10O5+6O2![]() 6CO2+5H2O
6CO2+5H2O
162 192
0.01g x
![]() =
=![]() ,x≈0.01185g
,x≈0.01185g
(3)由于0.01185g<0.092g因此该河中的鱼类不能维持生命.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】下面是一些关于铁的实验研究,试按要求填空.
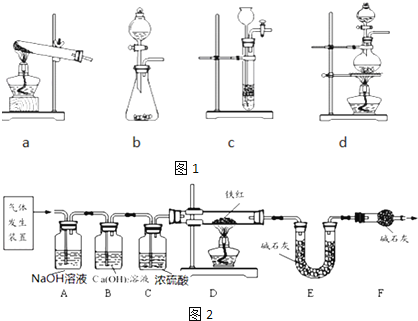
(1)模拟工业炼铁(装置图如图1):在硬质玻璃管内加入少量氧化铁粉末,先通入一氧化碳,排出装置内空气后,再用酒精喷灯加热A处药品.

①硬质玻璃管内发生反应的化学方程式为: .
②试管B中发生反应的化学方程式为: .
③该装置的主要缺点是 .
(2)铁锈蚀的探究
某化学兴趣小组进行家庭化学实验“探究铁锈蚀的原因”,设计如图2所示.他们预设的实验结果是仅有图Ⅲ中的铁钉生锈.但经过一周时间的观察,他们发现三支试管中铁钉都生锈了.
老师在听取了同学汇报后,做了如下实验帮助同学分析原因:取4份等量自来水样,经过不同的方法处理后,用数字传感器测定水样中的溶解氧,并进行如图2(Ⅰ、Ⅱ、Ⅲ)的实验.
水样溶解氧数据如下:
自来水 | 1号水样 | 2号水样 | 3号水样 | 4号水样 |
处理方法 | 不处理 | 煮沸 密封迅速冷却 | 煮沸 密封自然冷却 | 煮沸 敞口冷却 |
溶解氧(mg/L) | 5.37 | 0.52 | 0.66 | 3.44 |
[教师实验的现象记录(部分)]用2号水样进行的如图Ⅱ的实验中:一天后,铁钉有轻微生锈,从第二天到第七天,铁锈不再增加.
参考所给数据分析:①学生实验中:图Ⅰ中铁钉生锈的原因可能是 ;
图Ⅱ中铁钉生锈的原因可能是 .
②教师实验所记录的实验现象的原因可能是 .
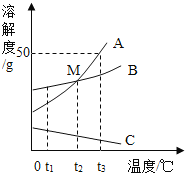
【题目】物质M在不同温度下的溶解度数据如下表所示,以下说法正确的是
温度/℃ | 0 | 20 | 40 | 60 | 80 |
溶解度/g | 12.6 | 15.3 | 20.0 | 25.0 | 38.2 |
A.0℃时,15.9 g M溶于150 g水中形成饱和溶液
B.20℃时,M形成饱和溶液的溶质质量分数是15.3%
C.若要配制200.0 g 20.0%的M的饱和溶液,对应温度必须是60℃
D.80℃时,M的饱和溶液138.2 g降温至40℃,析出晶体的质量大于20.0 g