题目内容
(2008?泸州)乙醇汽油就是在汽油中加入适量酒精混合而成的一种燃料.乙醇完全燃烧的化学方程式为C2H6O+3O2 2CO2+3H2O.
2CO2+3H2O.试回答下列问题:(计算结果保留一位小数)
(1)乙醇的相对分子质量为______.
(2)乙醇中碳、氢、氧元素的质量比是______.
(3)乙醇中碳元素的质量分数是______.
(4)完全燃烧100g乙醇,能生成二氧化碳多少克?
【答案】分析:(1)相对分子质量为化学式中各元素的相对原子质量的总和;
(2)组成元素质量比为各元素的相对原子质量与原子个数的乘积之比;
(3)组成元素的质量分数= ×100%;
×100%;
(4)根据反应的化学方程式,由反应物乙醇的物质计算生成二氧化碳的质量.
解答:解:(1)乙醇C2H6O的相对分子质量=12×2+1×6+16=46
故答案为:46;
(2)乙醇C2H6O中碳、氢、氧元素的质量比=(12×2):(1×6):16=12:3:8
故答案为:12:3:8;
(3)乙醇C2H6O中碳元素的质量分数=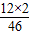 ×100%≈52.2%
×100%≈52.2%
故答案为:52.2%;
(4)设完全燃烧100g乙醇,能生成二氧化碳的质量为x
C2H6O+3O2 2CO2+3H2O
2CO2+3H2O
46 88
100g x
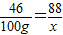 解之得x≈191.3g
解之得x≈191.3g
答:完全燃烧100g乙醇,能生成二氧化碳的质量为191.3g.
点评:完全燃烧100g乙醇,能生成二氧化碳的质量也可以根据化学变化前后元素质量不数,利用化学式的计算进行解决:
完全燃烧100g乙醇生成二氧化碳的质量=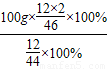 ≈191.3g.
≈191.3g.
(2)组成元素质量比为各元素的相对原子质量与原子个数的乘积之比;
(3)组成元素的质量分数=
 ×100%;
×100%;(4)根据反应的化学方程式,由反应物乙醇的物质计算生成二氧化碳的质量.
解答:解:(1)乙醇C2H6O的相对分子质量=12×2+1×6+16=46
故答案为:46;
(2)乙醇C2H6O中碳、氢、氧元素的质量比=(12×2):(1×6):16=12:3:8
故答案为:12:3:8;
(3)乙醇C2H6O中碳元素的质量分数=
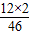 ×100%≈52.2%
×100%≈52.2%故答案为:52.2%;
(4)设完全燃烧100g乙醇,能生成二氧化碳的质量为x
C2H6O+3O2
 2CO2+3H2O
2CO2+3H2O46 88
100g x
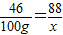 解之得x≈191.3g
解之得x≈191.3g答:完全燃烧100g乙醇,能生成二氧化碳的质量为191.3g.
点评:完全燃烧100g乙醇,能生成二氧化碳的质量也可以根据化学变化前后元素质量不数,利用化学式的计算进行解决:
完全燃烧100g乙醇生成二氧化碳的质量=
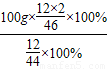 ≈191.3g.
≈191.3g. 
练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
 ”、“
”、“ ”表示不同的原子,请根据图示回答下列问题:
”表示不同的原子,请根据图示回答下列问题:
