题目内容
用稀盐酸和溶质质量分数为40%的氢氧化钠进行中和反应的实验,将稀盐酸逐滴加入到10.0g氢氧化钠溶液中,边滴加边搅拌,随着稀盐酸的滴加,溶液的pH变化情况如图所示(不考虑反应过程中热量散失):
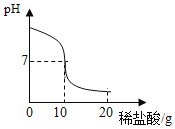
(1)当pH=7时,烧杯中的溶质是________。
(2)计算稀盐酸中溶质的质量分数(精确到0.1%)____。
“见著知徽,见微知著”是一种常见的化学思维方法。对下列事实用微粒的知识解释不正确的是( )
选项 | 事实 | 解释 |
A | 水和过氧化氢有不同的化学性质 | 构成物质的分子不同 |
B | 自然界中的水有三态变化 | 水分子的大小随温度改变而改变 |
C | 自然界中,金刚石最硬,但石墨质软 | 碳原子排列方式不同 |
D | 酸、碱、盐溶液都能导电 | 溶液中有自由移动的离子 |
A.A B.B C.C D.D
某化学兴趣小组的同学在学习九年级《化学》下册中的资料卡片“石笋和钟乳石的形成”时,发现难溶于水的碳酸钙当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O═Ca(HCO3)2,联想到实验室中澄清石灰水与二氧化碳反应会生成碳酸钙:Ca(OH)2+CO2═CaCO3↓+H2O,对长时间向碱溶液中通入CO2,反应后溶液中的溶质组成产生了浓厚的兴趣。
(提出问题)一定量CO2与NaOH溶液反应后的溶质组成是什么?
(查阅资料)
(1)通入少量CO2反应的化学方程式为______。
(2)通入过量CO2,反应的化学方程式为Na2CO3+CO2+H2O═2NaHCO3。
(3)碳酸氢盐都是可溶于水的,BaCO3难溶于水。
(4)碳酸氢钠溶液呈碱性。
(提出猜想)
(1)溶质为NaOH和Na2CO3;
(2)溶质为Na2CO3;
(3)溶质为______(填化学式);
(4)溶质为NaHCO3。
(设计实验)
实验步骤 | 实验现象 | 实验结论 |
(1)用玻璃棒蘸取反应后溶液,滴在pH试纸上 | pH=9 | 该溶液显 ______ 性 |
(2)取反应后溶液少许于试管中,向其中滴加过量的BaCl2溶液 | 有 ______ 生成 | 猜想(4)不成立 |
(3)取步骤(2)中的上层清液,滴入稀盐酸 | 有气泡冒出 | 猜想 ______ 不成立 |
(得出结论)猜想(3)成立。
(讨论交流)
(1)有同学提出,实验步骤(1)是多余的。你认为该实验设计是否需要?______(填“需要”或“不需要”)。
(2)同学们又一次把目光投向了教材,发现遇热或压强变小时:Ca(HCO3)2═CaCO3↓+CO2↑+H2O,纷纷提出,干粉灭火器中用NaHCO3灭火的反应原理与之相似,试写出NaHCO3受热分解的化学方程式:______ 。
(反思应用)向澄清石灰水中不断通入二氧化碳,观察到的现象是______。


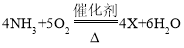 ,则X的化学式为( )
,则X的化学式为( )