题目内容
 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.
①自来水厂净水过程中需加消毒剂.高铁酸钾(K2FeO4)是一种高效的消毒剂,其中铁元素的化合价为________.
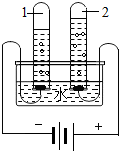
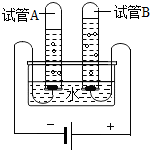
②在如图电解水实验过程中发生改变的微粒是________(填名称),当其中一个电极产生4mL气体时,另一电极产生的气体体积可能是________mL.
③许多化学实验中都要用到水,做细铁丝在氧气中燃烧的实验时,集气瓶中盛少量水的目是________,写出该反应的化学方程式:________.
④实验室常用水稀释浓溶液.Ⅰ.实验室若用100mL 98%的浓硫酸(密度为1.84g/cm3)配制20%的稀硫酸,需要蒸馏水(密度为1g/cm3)为________mL.Ⅱ.在其它操作无误情况下,用量筒量取浓硫酸时仰视读数,所配溶液溶质质量分数________ 20%(填“小于”、“大于”或“等于”).
+6 水分子 2或8 防止生成物溅落炸裂瓶底 3Fe+2O2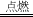 Fe3O4 717.6 大于
Fe3O4 717.6 大于
分析:①根据化合物中各元素化合价的代数和为0进行解答;
②根据电解水实验过程中发生改变的微粒是水分子以及氢气和氧气的体积比为2:1进行解答;
③根据铁丝在氧气中燃烧生成四氧化三铁以及注意事项进行解答;
④根据溶液稀释过程中溶质不变进行解答.
解答:①由化合物中各元素化合价的代数和为0以及高铁酸钾(K2FeO4)中钾元素的化合价为+1价、氧元素的化合价为-2价,所以铁元素的化合价为+6价;故填:+6;
②电解水实验过程中发生改变的微粒是水分子,氢气和氧气的体积比为2:1,所以当其中一个电极产生4mL气体时,另一电极产生的气体体积可能是2或8mL;故填:水分子;2或8;
③铁丝在氧气中燃烧生成四氧化三铁,该反应的化学方程式:3Fe+2O2 Fe3O4,集气瓶中盛少量水的目是防止生成物溅落炸裂瓶底;故填:防止生成物溅落炸裂瓶底;3Fe+2O2
Fe3O4,集气瓶中盛少量水的目是防止生成物溅落炸裂瓶底;故填:防止生成物溅落炸裂瓶底;3Fe+2O2 Fe3O4;
Fe3O4;
④设需要蒸馏水的质量为x.
100mL×98%×1.84g/cm3=(100mL×1.84g/cm3+x)×20%
x=717.6g
需要蒸馏水的体积(密度为1g/cm3)为=717.6g/1g/cm3=717.6mL
在其它操作无误情况下,用量筒量取浓硫酸时仰视读数,会使得浓硫酸的体积大于100mL,所配溶液溶质质量分数大于20%.故填:717.6;大于.
点评:本题为涉及较多的化学基础知识,题目难点不大但涉及面较广,耐心审题、沉着作答对于解答类似问题会有较大帮助.
 Fe3O4 717.6 大于
Fe3O4 717.6 大于分析:①根据化合物中各元素化合价的代数和为0进行解答;
②根据电解水实验过程中发生改变的微粒是水分子以及氢气和氧气的体积比为2:1进行解答;
③根据铁丝在氧气中燃烧生成四氧化三铁以及注意事项进行解答;
④根据溶液稀释过程中溶质不变进行解答.
解答:①由化合物中各元素化合价的代数和为0以及高铁酸钾(K2FeO4)中钾元素的化合价为+1价、氧元素的化合价为-2价,所以铁元素的化合价为+6价;故填:+6;
②电解水实验过程中发生改变的微粒是水分子,氢气和氧气的体积比为2:1,所以当其中一个电极产生4mL气体时,另一电极产生的气体体积可能是2或8mL;故填:水分子;2或8;
③铁丝在氧气中燃烧生成四氧化三铁,该反应的化学方程式:3Fe+2O2
 Fe3O4,集气瓶中盛少量水的目是防止生成物溅落炸裂瓶底;故填:防止生成物溅落炸裂瓶底;3Fe+2O2
Fe3O4,集气瓶中盛少量水的目是防止生成物溅落炸裂瓶底;故填:防止生成物溅落炸裂瓶底;3Fe+2O2 Fe3O4;
Fe3O4;④设需要蒸馏水的质量为x.
100mL×98%×1.84g/cm3=(100mL×1.84g/cm3+x)×20%
x=717.6g
需要蒸馏水的体积(密度为1g/cm3)为=717.6g/1g/cm3=717.6mL
在其它操作无误情况下,用量筒量取浓硫酸时仰视读数,会使得浓硫酸的体积大于100mL,所配溶液溶质质量分数大于20%.故填:717.6;大于.
点评:本题为涉及较多的化学基础知识,题目难点不大但涉及面较广,耐心审题、沉着作答对于解答类似问题会有较大帮助.

练习册系列答案
相关题目
水是生命的源泉,也是不可缺少的资源。
(1)某矿泉水的主要矿物质成分及含量如下表:
| 成分 | Ca | K | Zn | F |
| 含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注。请参与讨论下列有关问题:
(Ⅰ)自来水、蒸馏水、海水中属于纯净物的是 。
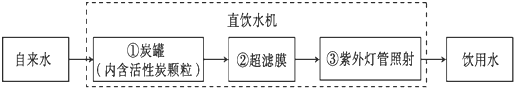
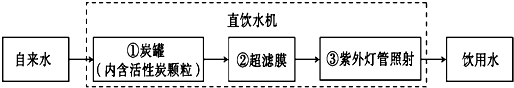
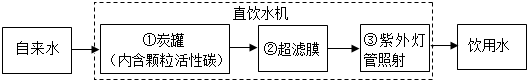
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如下图所示:
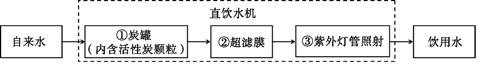
①对应的作用是 (填字母序号,下同),③对应的作用是 。
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有 。
A.大量使用化肥、农药 B.工业废气处理后排放 C.禁止使用含磷洗衣粉
(Ⅳ)能确认水是由氧元素和氢元素组成的实验是 。
A.水的蒸发 B.水的电解 C.水的净化

 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.