题目内容
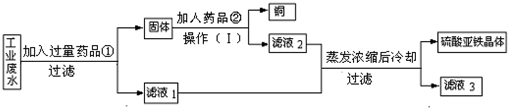
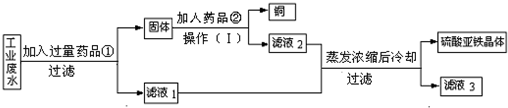
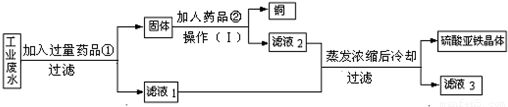
有一种工业废水,已知其中含有大量硫酸亚铁,少量硫酸铜和硫酸钠.今设计一种既经济又合理的方法,回收铜和硫酸亚铁.可使用的药品:铁、铜、稀硫酸、稀盐酸.设计方案与实验过程如图所示:
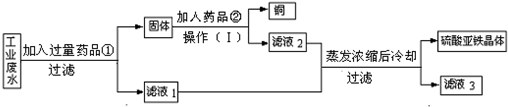
根据实验过程判断:
(1)写出加入药品①后发生的反应的化学方程式
(2)加入药品②与操作(Ⅰ)的目的是
a.分离出铜和增加滤液①b.除去过量的药品①和分离出铜 c.除去过量的药品①和增加滤液①

根据实验过程判断:
(1)写出加入药品①后发生的反应的化学方程式
Fe+CuSO4═Cu+FeSO4
Fe+CuSO4═Cu+FeSO4
.(2)加入药品②与操作(Ⅰ)的目的是
b
b
(用编号表示).a.分离出铜和增加滤液①b.除去过量的药品①和分离出铜 c.除去过量的药品①和增加滤液①
分析:(1)根据实验目的要收集铜和硫酸亚铁,所以应加入过量的铁来置换出铜,可以据此解答;
(2)由于加入过量的铁,所以为了将铁转化为硫酸亚铁,应该加入稀硫酸来将多余的铁反应掉,可以据此解答.
(2)由于加入过量的铁,所以为了将铁转化为硫酸亚铁,应该加入稀硫酸来将多余的铁反应掉,可以据此解答.
解答:解:(1)根据实验目的要收集铜和硫酸亚铁,所以应加入过量的铁来置换出铜,铁和硫酸铜反应生成了铜和硫酸亚铁,可以写出该反应的化学方程式为:Fe+CuSO4═Cu+FeSO4;
(2)由于加入过量的铁,所以为了将铁转化为硫酸亚铁,应该加入稀硫酸来将多余的铁反应掉,同时可得到较纯的铜,故该实验目的为b.
故答案为:
(1)Fe+CuSO4═Cu+FeSO4;
(2)b.
(2)由于加入过量的铁,所以为了将铁转化为硫酸亚铁,应该加入稀硫酸来将多余的铁反应掉,同时可得到较纯的铜,故该实验目的为b.
故答案为:
(1)Fe+CuSO4═Cu+FeSO4;
(2)b.
点评:不溶于液体的固体与液体分离的方法是过滤,从溶液中得到一种金属时,加入排在该金属前面的金属利用置换反应就行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目