题目内容
现有镁、铁锈、氯化铜溶液、稀硫酸、石灰水等五种物质,从这五种物质中任意选取物质,按下列要求写出化学方程式;
①有气体生成
②有蓝色沉淀生成
③有水生成但不是中和反应 .
①有气体生成
②有蓝色沉淀生成
③有水生成但不是中和反应
考点:书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:根据置换反应的定义和生成物的要求进行分析;根据复分解反应中生成物的要求进行分析;
解答:解:①镁和硫酸反应生成硫酸镁和氢气的反应是生成了气体的置换反应,故答案为:Mg+H2SO4═MgSO4+H2↑;
②氯化铜和石灰水生成氢氧化铜沉淀,故答案为:CuCl2+Ca(OH)2═CaCl2+Cu(OH)2↓;
③有水生成但不是中和反应的是铁锈和稀硫酸反应,故答案为:Fe2O3+3H2SO4=Fe2(SO4)3+3H20
②氯化铜和石灰水生成氢氧化铜沉淀,故答案为:CuCl2+Ca(OH)2═CaCl2+Cu(OH)2↓;
③有水生成但不是中和反应的是铁锈和稀硫酸反应,故答案为:Fe2O3+3H2SO4=Fe2(SO4)3+3H20
点评:在解此类题时,首先分析所给物质的性质,然后结合方程式要求的和质量守恒定律进行书写.

练习册系列答案
相关题目
实验室里配制溶质质量分数为2%NaOH溶液200g(密度近似1.0g/mL),下列实验操作不正确的是( )
| A、选用100mL量筒量取98.0mL水 |
| B、将NaOH固体放入小烧杯中,用托盘天平称取2.0gNaOH |
| C、将准确称取的NaOH固体直接倒入装有水的量筒中溶解 |
| D、10ml溶质质量分数为2%的NaOH溶液加入10mL水稀释得到1%NaOH溶液 |
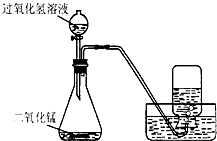 如图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表.
如图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表.
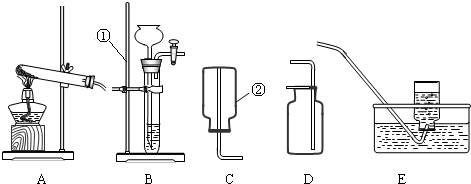
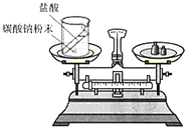 请根据题目要求回答下列问题.
请根据题目要求回答下列问题.