题目内容
【题目】水蒸气能与铁粉在高温下反应,生成氢气和铁的一种氧化物X.为验证生成物的成分,现称量一定量铁粉,进行如下实验。
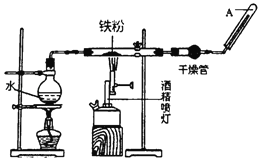
(1)收集氢气的试管口向下是因为_____,点燃氢气前应先检验_____
(2)氧化物X的成分确定:
(初步判断)已知铁的氧化物中氧化亚铁、四氧化三铁均为黑色、氧化铁为红色,且只有四氧化三铁能被磁铁吸引。写出判断氧化物成分的简单方法_____。
(定量测量)通过测定氧化物X中铁、氧两元素质量比,可确定氧化物X的种类。简要写出测定方法__。若氧化物X为四氧化三铁,反应的化学方程式为___。
【答案】氢气的密度比空气小 氢气的纯度 先观察颜色,后用磁铁吸引 实验前先称量出玻璃管内铁粉的质量,在实验结束装置冷却至室温后,再称量玻璃管内固体的质量 3Fe+4H2O![]() Fe3O4+4H2↑
Fe3O4+4H2↑
【解析】
(1)氢气的密度比空气小,所以收集氢气时,试管口要向下倾斜;氢气具有可燃性,不纯的氢气点燃可能会发生爆炸,所以点燃氢气前应先检验氢气的纯度;故填:氢气的密度比空气小;氢气的纯度;
(2)[初步判断]先观察生成物的颜色,若为红色,则是氧化铁;若是黑色,再用磁铁吸引,若能被磁铁吸引则是四氧化三铁,若不能被吸引则是氧化亚铁;故填:先观察颜色,后用磁铁吸引;
[定量测量]
实验前先称量出玻璃管内铁粉的质量,在实验结束装置冷却至室温后,再称量玻璃管内固体的质量,固体质量的质量就是氧化物中氧元素的质量,进一步计算出氧化物中铁、氧原子个数比,最后确定化学式;水蒸气和铁在高温的条件下反应生成四氧化三铁和氢气;故填:实验前先称量出玻璃管内铁粉的质量,在实验结束装置冷却至室温后,再称量玻璃管内固体的质量;3Fe+4H2O![]() Fe3O4+4H2↑。
Fe3O4+4H2↑。

练习册系列答案
相关题目