��Ŀ����
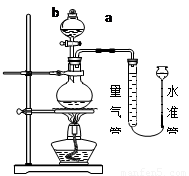
ʵ���ҳ��ü��ȣ�85�棩NH4Cl��NaNO2���ֱ�����Һ�ķ�����ȡN2����ͼ��ʵ���������ַ�����N2�����ⶨ����N2�����װ�ã�����װ����ȥ������ش�������⣺
���������ϡ���
1��NH4Cl��NaNO2��Ӧ����NaCl��H2O��N2�����ų�����������
2��20��ʱ��NH4Cl���ܽ��ԼΪ37g��
3��N2������ˮ��ʵ�������£��ܶ�Ϊ1.25g��L��1��
��ʵ�鲽�衿��
�� ��
��20��ʱ��ȡ0.78g����NH4Cl��Һ������ƿ������װ�ã�
�۵���ˮ�ܣ�ʹ������������Һ����ƽ����¼��������ˮ�����Ϊ12mL��
�ܴ�Һ©����������ε��뱥��NaNO2��Һ����������Ӧ���������߾ƾ��ƣ�
����ƿ�в��ٲ�������ʱ���رջ�����
����ȴ�����£���������Һ��߶���ƽ����¼��������ˮ�����ΪV mL��
�ߴ���ʣ��ҩƷ������ʵ��̨��
��ʵ����������ݴ�������
��1��д��װ�������������ƣ�a�� ��b�� ��
��2����Ӧ�Ļ�ѧ����ʽΪ�� ��
��3������ʵ�鲽���е���ȱ���֣��� ��
��4��������У����߾ƾ��Ƶ�Ŀ���� ��
��5��NH4Cl��һ�� ������ܡ��������ܡ������ܡ��������ܡ������ʡ�20��ʱ���䱥����Һ��������������Ϊ ������ʵ�����ݼ��㣬���ɵ���ԼΪ���ٺ�������3�֣���������У��м����ݱ���2λС�������ս��Ϊ��������Է���������Mr-NH4Cl��53.5��Mr-N2��28��
��6�����ݼ��������������V����ֵΪ ��
��7��ʵ���У�ʵ�ʲ�õ��������ƫ����ԭ���� ��
A��ʵ���м��뱥��NaNO2��Һ�����Ҳ����Ϊ����N2�����
B��װ��©��
��1��a����Һ©�� b������̨ ��2��NaNO2 + NH4Cl = NaCl + 2H2O + N2�� ��3����������� ��4����Ϊ��Ӧ���ȣ���ֹˮ����ˮ�����Ӱ��ʵ�飨����д���ؼ��ʡ���Ӧ���ȡ��� ��5������ 27�� 88ml ��6��100 ��7��A
��������
�����������1��д��װ�������������ƣ�a����©����b����̨����2����Ӧ�Ļ�ѧ����ʽΪNaNO2 + NH4Cl = NaCl + 2H2O + N2������3������ʵ�鲽���е���ȱ���֣��ټ�������ԣ���4��������У����߾ƾ��Ƶ�Ŀ������Ϊ��Ӧ���ȣ���ֹˮ����ˮ�����Ӱ��ʵ�飻��5��NH4Cl��һ������20��ʱ���䱥����Һ��������������Ϊ37/137��100%=27%
�⣺ 0.78g����NH4Cl��Һ�У�NH4Cl������Ϊ��0.78��27�� �� 0.21g
�跴Ӧ����N2������Ϊx
NaNO2 + NH4Cl = NaCl + 2H2O + N2��
53.5 28
0.21g x
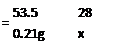
x �� 0.11g
�� ʵ������N2����� =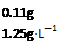 =88mL
=88mL
��6�����ݼ��������������V����ֵΪ��Ϊ��ʼʱ��������Ϊ12ml����������Ϊ88ml���������Ϊ100ml����7��ʵ���У�ʵ�ʲ�õ��������ƫ����ԭ����A��ʵ���м��뱥��NaNO2��Һ�����Ҳ����Ϊ����N2�����.
���㣺ʵ��̽��������������

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
 ʵ���ҳ��ü��ȣ�85�棩NH4Cl��NaNO2���ֱ�����Һ�ķ�����ȡN2����ͼ��ʵ���������ַ�����N2�����ⶨ����N2�����װ�ã�����װ����ȥ������ش�������⣺
ʵ���ҳ��ü��ȣ�85�棩NH4Cl��NaNO2���ֱ�����Һ�ķ�����ȡN2����ͼ��ʵ���������ַ�����N2�����ⶨ����N2�����װ�ã�����װ����ȥ������ش�������⣺