题目内容
我国是世界上少数以煤为主要能源的国家,70%左右的能源要靠煤来供给,燃烧含硫的煤会向空气中排放大量的SO2,导致酸雨的发生.目前全世界的燃煤工厂和发电厂都普遍应用湿净化器对煤燃烧后产生的烟气脱硫,主要反应原理为:2SO2+2CaCO3+4H2O+O2=2CO2+2CaSO4?2H2O (石膏)
某厂现有125t含杂质20%的石灰石,若运用上述反应原理吸收SO2气体,则最多可以吸收SO2气体多少吨?(杂质不参加反应)
【答案】分析:根据化学方程式中反应物和生成物之间的质量比可以进行正确的计算.
解答:解:125t含杂质20%的石灰石中碳酸钙的质量为:125t×(1-20%)=100t
设最多可以吸收SO2气体的质量为X.
2SO2+2CaCO3+4H2O+O2=2CO2+2CaSO4?2H2O
128 200
X 100t
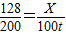
X=64t
答:最多可以吸收SO2气体的质量为64t.
点评:解答本题要紧紧围绕化学方程式及其反应物和生成物的质量关系进行正确的计算.
解答:解:125t含杂质20%的石灰石中碳酸钙的质量为:125t×(1-20%)=100t
设最多可以吸收SO2气体的质量为X.
2SO2+2CaCO3+4H2O+O2=2CO2+2CaSO4?2H2O
128 200
X 100t
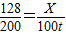
X=64t
答:最多可以吸收SO2气体的质量为64t.
点评:解答本题要紧紧围绕化学方程式及其反应物和生成物的质量关系进行正确的计算.

练习册系列答案
相关题目