题目内容
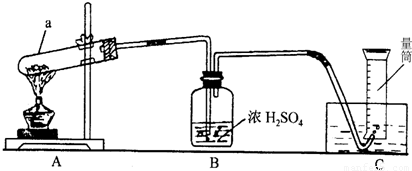
有一批混有MnO2的KMnO4样品.一位同学设计如图所示的实验装置去检验其纯度.取4.00g样品放入图a中充分加热,直到反应完全,并用如图的装置测量出生成氧气的体积.(氧气的密度为1.43g/L,溶于水的气体体积忽略不计.)
请回答:

(1)写出a仪器名称
(2)指出A装置中的一处错误是
(3)撤去B装置对实验结果有没有影响
(4)改正A的错误后,A的装置还可用作下列哪一种气体制取
A.加热氯化铵固体和熟石灰的混合物制NH3
B.稀盐酸和石灰石混合制取CO2
C.稀硫酸和锌粒混合制取H2
(5)反应结束后,量筒内液面处于224mL刻度处(量筒内外高度一致),则气体质量为
请回答:

(1)写出a仪器名称
试管
试管
;(2)指出A装置中的一处错误是
试管口向上倾斜了,应该略向下倾斜
试管口向上倾斜了,应该略向下倾斜
;(3)撤去B装置对实验结果有没有影响
有
有
(填“有”或“无”),原因是氧气中混有水蒸气
氧气中混有水蒸气
;(4)改正A的错误后,A的装置还可用作下列哪一种气体制取
A
A
;A.加热氯化铵固体和熟石灰的混合物制NH3
B.稀盐酸和石灰石混合制取CO2
C.稀硫酸和锌粒混合制取H2
(5)反应结束后,量筒内液面处于224mL刻度处(量筒内外高度一致),则气体质量为
0.32
0.32
g,原混合物中高锰酸钾的质量分数约为79%
79%
.分析:(1)根据试管是常见的仪器常用于气体的制取分析.
(2)根据为防止水倒流炸裂试管所以试管口要略向下倾斜分析.
(3)根据B中的浓硫酸能除去氧气中的水蒸气分析.
(4)根据该装置适合用固体加热制取气体分析.
(5)根据密度乘以体积即可求出氧气的质量,然后根据高锰酸钾制氧气的化学方程式求出高锰酸钾的质量,除以4g乘以100%即可求解.
(2)根据为防止水倒流炸裂试管所以试管口要略向下倾斜分析.
(3)根据B中的浓硫酸能除去氧气中的水蒸气分析.
(4)根据该装置适合用固体加热制取气体分析.
(5)根据密度乘以体积即可求出氧气的质量,然后根据高锰酸钾制氧气的化学方程式求出高锰酸钾的质量,除以4g乘以100%即可求解.
解答:解:(1)试管常用于气体的制取,故答案:试管.
(2)为防止水倒流炸裂试管所以试管口要略向下倾斜,故答案:试管口向上倾斜了,应该略向下倾斜.
(3)B中的浓硫酸具有吸水性,能除去氧气中的水蒸气,故答案:有;氧气中混有水蒸气.
(4)该装置适合用固体加热制取气体,故选A..
(5)生成氧气的质量:1.43g/L×0.224mL=0.32g
设样品中高锰酸钾的质量为x
2KMnO4
K2MnO4+MnO2+O2↑
316 32
x 0.32g
=
x=3.16g
×100%=79%
故答案:0.32g;79%.
(2)为防止水倒流炸裂试管所以试管口要略向下倾斜,故答案:试管口向上倾斜了,应该略向下倾斜.
(3)B中的浓硫酸具有吸水性,能除去氧气中的水蒸气,故答案:有;氧气中混有水蒸气.
(4)该装置适合用固体加热制取气体,故选A..
(5)生成氧气的质量:1.43g/L×0.224mL=0.32g
设样品中高锰酸钾的质量为x
2KMnO4
| ||
316 32
x 0.32g
| 316 |
| x |
| 32 |
| 0.32g |
x=3.16g
| 3.16g |
| 4g |
故答案:0.32g;79%.
点评:考查了用高锰酸钾制取氧气时操作中应该注意的问题和根据高锰酸钾制取氧气的化学方程式的计算,计算时一定要细心算对氧气的质量才能保证后面的求解正确.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目