题目内容
 (2009?湖北)A、B、H为固体单质,E为黑色固体,F为赤铁矿的主要成分,K为蓝色的硫酸盐溶液.它们之间有如图所示转化关系.
(2009?湖北)A、B、H为固体单质,E为黑色固体,F为赤铁矿的主要成分,K为蓝色的硫酸盐溶液.它们之间有如图所示转化关系.请回答:
(1)写出下列物质的化学式:A
C
C
;ECuO
CuO
.(2)写出下列转化的化学方程式:D+F═H+C
3CO+Fe2O3
2Fe+3CO2
| ||
3CO+Fe2O3
2Fe+3CO2
;H
| ||
| K |
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
.(3)如图所示的转化关系中不属于置换反应的有
2
2
个.分析:本题属于推断题,根据题目给出的流程图和信息:F为赤铁矿的主要成分,因此F是氧化铁,金属氧化物在初中阶段只能与酸和还原剂反应,A、B、H为固体单质,因此A是单质碳,碳和氧化铁在高温的条件下生成铁和二氧化碳,E为黑色固体,因此E是氧化铜,碳和氧化铜在高温的条件下生成铜和二氧化碳,因此B是铜,C是二氧化碳,H是铁;K为蓝色的硫酸盐溶液,铁和硫酸铜溶液反应生成硫酸亚铁和铜,因此K是硫酸铜;D与氧化铁和氧化铜都能反应生成二氧化碳,因此D是一氧化碳.
解答:解:(1)F为赤铁矿的主要成分,因此F是氧化铁,金属氧化物在初中阶段只能与酸和还原剂反应,A、B、H为固体单质,因此A是单质碳,碳和氧化铁在高温的条件下生成铁和二氧化碳,E为黑色固体,因此E是氧化铜,也能被碳还原,故答案为:C;CuO;
(2)D与氧化铁和氧化铜都能反应生成二氧化碳,因此D是一氧化碳,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳;铁和硫酸铜溶液反应生成硫酸亚铁和铜;故答案为:3CO+Fe2O3
2Fe+3CO2;Fe+CuSO4=FeSO4+Cu;
(3)一氧化碳还原氧化铜和一氧化碳还原氧化铁的化学反应,都不是置换反应,因此有两个反应不属于置换反应;故答案为:2
(2)D与氧化铁和氧化铜都能反应生成二氧化碳,因此D是一氧化碳,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳;铁和硫酸铜溶液反应生成硫酸亚铁和铜;故答案为:3CO+Fe2O3
| ||
(3)一氧化碳还原氧化铜和一氧化碳还原氧化铁的化学反应,都不是置换反应,因此有两个反应不属于置换反应;故答案为:2
点评:本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.本考点是中考的重要内容之一,一般有两种类型:一是图框式推断题;二是文字描述型推断题;本题属于第一种类型.不论哪一种类型,都是通过实验现象,从而得出物质的组成.此考点主要出现在填空题和实验题中.

练习册系列答案
相关题目
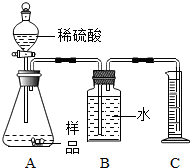 (2009?湖北)烧碱是常用的消毒剂,因烧碱价廉而被广泛地应用,工业烧碱中常常因含有Na2CO3杂质而不纯.甲、乙两同学设计实验来探究工业烧碱中NaOH的质量分数.
(2009?湖北)烧碱是常用的消毒剂,因烧碱价廉而被广泛地应用,工业烧碱中常常因含有Na2CO3杂质而不纯.甲、乙两同学设计实验来探究工业烧碱中NaOH的质量分数.