题目内容
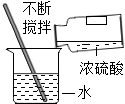
【题目】海洋是巨大的资源宝库,小华模拟化工厂的生产流程,以海水和贝壳(主要成分是CaCO3)为主要原料,生产金属镁,其设计工艺流程如图1
(1)要将Mg(OH)2沉淀分离出来,操作甲的名称是 . 如果在实验室中完成该操作,要用到玻璃棒,其作用是 .
(2)试剂A是一种溶液,其溶质是(填化学式).生产上制备物质都有工艺流程图,例如生产CuSO4的工艺流程图如下:
Cu ![]() CuO
CuO ![]() CuSO4
CuSO4
请画出生产试剂A的工艺流程 .
(3)金属材料往往以合金的形式出现,有一块含镁的合金,为测定它的成分,将它碾成粉末,慢慢加入到100gHCl溶液中,产生气体与合金质量的关系如图2所示:
下列说法正确的是
A.若是镁铝合金,则m>0.2g
B.若是镁铁合金,则m>0.2g
C.若是镁铜合金,则m=0.2g
D.若是镁锌合金,则HCl溶液的质量分数小于7.3%
【答案】
(1)过滤,引流
(2)Ca(OH)2,CaCO3 ![]() CaO
CaO ![]() Ca(OH)2
Ca(OH)2
(3)A
【解析】解:(1)要将Mg(OH)2沉淀分离出来,采用的方法是过滤.此过程中玻璃棒的作用是引流;所以答案是:过滤;引流.(2)试剂a是氢氧化钙溶液,其溶质是Ca(OH)2,加入该试剂时发生反应的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.所以答案是:Ca(OH)2;
高温煅烧石灰石,生成氧化钙,氧化钙再与水反应生成氢氧化钙;故填:CaCO3 ![]() CaO
CaO ![]() Ca(OH)2;(3)假设2.4g镁与盐酸反应生成氢气的质量为x,需要HCl的质量为y
Ca(OH)2;(3)假设2.4g镁与盐酸反应生成氢气的质量为x,需要HCl的质量为y
Mg+ | 2HCl=MgCl2 + | H2↑ |
24 | 73 | 2 |
2.4g | y | x |
![]()
x=0.2g
y=7.3g
等质量的镁、铝、铁与足量的盐酸反应生成氢气的多少可根据: ![]() 来分析,此比值越小,生成的氢气越多,
来分析,此比值越小,生成的氢气越多,
镁: ![]() ;铝:
;铝: ![]() ;铁:
;铁: ![]() =28,可见若是镁铝合金,则m>0.2g;若是镁铁合金,则m<0.2g;因此铜不与盐酸反应,所以若是镁铜合金,则m<0.2g;
=28,可见若是镁铝合金,则m>0.2g;若是镁铁合金,则m<0.2g;因此铜不与盐酸反应,所以若是镁铜合金,则m<0.2g;
此稀盐酸中,溶质的质量分数最小为: ![]() =7.3%.
=7.3%.
所以答案是:A.
【考点精析】根据题目的已知条件,利用过滤操作的注意事项的相关知识可以得到问题的答案,需要掌握过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损.

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案