题目内容
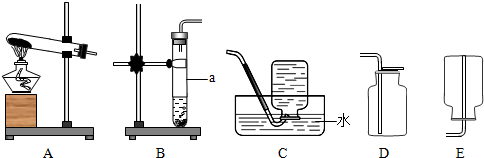
请结合图里所示实验装置回答有关问题: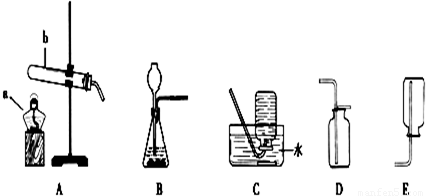
(1)写出装置A中标号a和b的仪器名称:a ;b .
(2)检查装置B的气密性的方法是:将该装置中的导气管用弹簧夹夹住,往长颈漏斗中注入水至液面高出长颈漏斗的下端管口,若能观察到 现象,即可证明装置不漏气.
(3)小丽用高锰酸钾制取氧气时,应选用的发生装置是 ,收集装置应选择 ,反应的化学方程式为 .用排水法收集氧气完毕后,停止加热时的顺序是先 ,然后 ,以防止水倒吸进入热的试管中,造成试管破裂.若水槽里的水变红了,原因是 .
(4)小红用过氧化氢和二氧化锰混合制取氧气,反应的化学方程式为 .反应装置选 .
(5)实验室制备CO2气体,用 来检验CO2,反应的化学方程式是 .
(6)实验室用固体亚硫酸钠和稀硫酸反应来制取SO2 气体,已知SO2是无色有毒气体,能溶于水.则实验室制取SO2气体的发生装置应选用 ,收集装置应选用 .
【答案】分析:(1)熟练掌握常见化学仪器的名称及其用途;
(2)依据检查装置B的气密性的方法回答;
(3)根据反应物的状态和反应条件选择发生装置:装置A适合固体加热型的气体制取,装置B适合固体和液体在常温下反应;根据气体的密度和溶解性选择收集方法;
用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,根据化学方程式的书写步骤书写方程式;根据实验操作的步骤及注意事项分析;
(4)实验室用过氧化氢溶液和二氧化锰制取氧气,二氧化锰是催化剂,写出反应的方程式;根据反应物的状态和反应条件选择发生装置;
(5)二氧化碳可以使石灰水变浑浊,以此来检验二氧化碳;
(6)根据反应物的状态和反应条件选择发生装置;根据气体的密度和溶解性选择收集方法.
解答:解:(1)a是酒精灯;b是试管;
(2)检查装置B的气密性的方法是:将该装置中的导气管用弹簧夹夹住,往长颈漏斗中注入水至液面高出长颈漏斗的下端管口,若能观察到长颈漏斗内的液面高于锥形瓶内的液面,即可证明装置不漏气;
(3)当采用高锰酸钾制取氧气时,由于需要加热,所以发生装置为A,而氧气不易溶于水且密度大于空气,所以既可以用排水法收集,也可以用向上排空气法收集;用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,因此反应的化学方程式为:2KMnO4 K2MnO4+MnO2+O2↑;制备氧气结束时应该先移出导气管再熄灭酒精灯,以防止水倒吸进入热的试管中,造成试管破裂;加热高锰酸钾制氧气并用排水法收集,为防止高锰酸钾顺着导管进入水槽,导管口要放一团棉花;故水槽水变成红色可能是:导管口没加棉花;
K2MnO4+MnO2+O2↑;制备氧气结束时应该先移出导气管再熄灭酒精灯,以防止水倒吸进入热的试管中,造成试管破裂;加热高锰酸钾制氧气并用排水法收集,为防止高锰酸钾顺着导管进入水槽,导管口要放一团棉花;故水槽水变成红色可能是:导管口没加棉花;
(4)实验室用过氧化氢溶液和二氧化锰制取氧气,二氧化锰是催化剂,反应的化学方程式为:2H2O2 2H2O+O2↑;发生装置属于固液常温型的装置B装置;
2H2O+O2↑;发生装置属于固液常温型的装置B装置;
(5)检验二氧化碳用石灰水,因为二氧化碳可以使石灰水变浑浊,反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(6)实验室用固体亚硫酸钠和稀硫酸反应来制取SO2 气体,故发生装置属于固体和液体在常温下的反应B装置;因为SO2是无色有毒气体,能溶于水,故不能采用排水法收集,而二氧化硫的密度比空气大,故采用向上排空气法收集;
故答案为:(1)酒精灯;试管; (2)长颈漏斗内的液面高于锥形瓶内的液面;(3)A;C或D;2KMnO4 K2MnO4+MnO2+O2↑;移出导气管;熄灭酒精灯;试管口没加棉花;(4)2H2O2
K2MnO4+MnO2+O2↑;移出导气管;熄灭酒精灯;试管口没加棉花;(4)2H2O2 2H2O+O2↑;B;(5)澄清的石灰水;CO2+Ca(OH)2=CaCO3↓+H2O;(6)B;D.
2H2O+O2↑;B;(5)澄清的石灰水;CO2+Ca(OH)2=CaCO3↓+H2O;(6)B;D.
点评:本题考查了常见气体的制取装置、收集方法等的选择,并在此基础上进行拓展,关键是明确发生装置、收集方法选择的依据.
(2)依据检查装置B的气密性的方法回答;
(3)根据反应物的状态和反应条件选择发生装置:装置A适合固体加热型的气体制取,装置B适合固体和液体在常温下反应;根据气体的密度和溶解性选择收集方法;
用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,根据化学方程式的书写步骤书写方程式;根据实验操作的步骤及注意事项分析;
(4)实验室用过氧化氢溶液和二氧化锰制取氧气,二氧化锰是催化剂,写出反应的方程式;根据反应物的状态和反应条件选择发生装置;
(5)二氧化碳可以使石灰水变浑浊,以此来检验二氧化碳;
(6)根据反应物的状态和反应条件选择发生装置;根据气体的密度和溶解性选择收集方法.
解答:解:(1)a是酒精灯;b是试管;
(2)检查装置B的气密性的方法是:将该装置中的导气管用弹簧夹夹住,往长颈漏斗中注入水至液面高出长颈漏斗的下端管口,若能观察到长颈漏斗内的液面高于锥形瓶内的液面,即可证明装置不漏气;
(3)当采用高锰酸钾制取氧气时,由于需要加热,所以发生装置为A,而氧气不易溶于水且密度大于空气,所以既可以用排水法收集,也可以用向上排空气法收集;用高锰酸钾制氧气时,反应物是高锰酸钾,生成物是锰酸钾、二氧化锰、氧气,反应条件是加热,因此反应的化学方程式为:2KMnO4
 K2MnO4+MnO2+O2↑;制备氧气结束时应该先移出导气管再熄灭酒精灯,以防止水倒吸进入热的试管中,造成试管破裂;加热高锰酸钾制氧气并用排水法收集,为防止高锰酸钾顺着导管进入水槽,导管口要放一团棉花;故水槽水变成红色可能是:导管口没加棉花;
K2MnO4+MnO2+O2↑;制备氧气结束时应该先移出导气管再熄灭酒精灯,以防止水倒吸进入热的试管中,造成试管破裂;加热高锰酸钾制氧气并用排水法收集,为防止高锰酸钾顺着导管进入水槽,导管口要放一团棉花;故水槽水变成红色可能是:导管口没加棉花;(4)实验室用过氧化氢溶液和二氧化锰制取氧气,二氧化锰是催化剂,反应的化学方程式为:2H2O2
 2H2O+O2↑;发生装置属于固液常温型的装置B装置;
2H2O+O2↑;发生装置属于固液常温型的装置B装置;(5)检验二氧化碳用石灰水,因为二氧化碳可以使石灰水变浑浊,反应的方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
(6)实验室用固体亚硫酸钠和稀硫酸反应来制取SO2 气体,故发生装置属于固体和液体在常温下的反应B装置;因为SO2是无色有毒气体,能溶于水,故不能采用排水法收集,而二氧化硫的密度比空气大,故采用向上排空气法收集;
故答案为:(1)酒精灯;试管; (2)长颈漏斗内的液面高于锥形瓶内的液面;(3)A;C或D;2KMnO4
 K2MnO4+MnO2+O2↑;移出导气管;熄灭酒精灯;试管口没加棉花;(4)2H2O2
K2MnO4+MnO2+O2↑;移出导气管;熄灭酒精灯;试管口没加棉花;(4)2H2O2 2H2O+O2↑;B;(5)澄清的石灰水;CO2+Ca(OH)2=CaCO3↓+H2O;(6)B;D.
2H2O+O2↑;B;(5)澄清的石灰水;CO2+Ca(OH)2=CaCO3↓+H2O;(6)B;D.点评:本题考查了常见气体的制取装置、收集方法等的选择,并在此基础上进行拓展,关键是明确发生装置、收集方法选择的依据.

练习册系列答案
相关题目


 2H2O+O2↑
2H2O+O2↑