题目内容
根据实验装置图,回答下列问题:
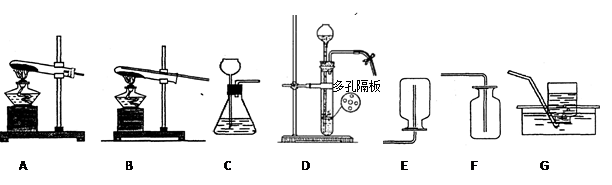
(1)图中标有a的仪器名称是 ;
(2)实验室用氯酸钾和二氧化锰制取较纯氧气的装置组合是 (填装置编号),化学方程式为 ;
(3)实验室用锌粒和稀硫酸制氢气, (填“能”或“不能”)用装置D作发生装置;
(4)氢气还原氧化铜的实验可选 装置(填装置编号);实验时发现试管破裂,分析其中原因可能是 ;
(5)根据实验室制取O2、CO2二种气体的反应原理、制取与收集方法。请你归纳出实验室制取气体反应的共同点 (填序号)。
①需要加热 ②使用催化剂 ③没有气体参加反应
④原料为纯净物 ⑤只生成一种气体
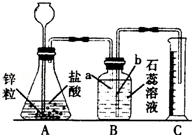
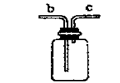
(6)若用下图装置进行排空气法收集二氧化碳气体,则气体应从 (填b或c)口进入;
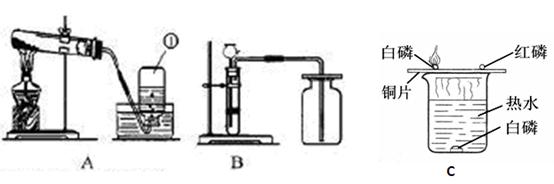
(7)下图是同学们在探究氧气性质实验中改进的实验装置图,简要回答甲、乙两个集气瓶中液体的作用 ,
。

(1)图中标有a的仪器名称是 ;
(2)实验室用氯酸钾和二氧化锰制取较纯氧气的装置组合是 (填装置编号),化学方程式为 ;
(3)实验室用锌粒和稀硫酸制氢气, (填“能”或“不能”)用装置D作发生装置;
(4)氢气还原氧化铜的实验可选 装置(填装置编号);实验时发现试管破裂,分析其中原因可能是 ;
(5)根据实验室制取O2、CO2二种气体的反应原理、制取与收集方法。请你归纳出实验室制取气体反应的共同点 (填序号)。
①需要加热 ②使用催化剂 ③没有气体参加反应
④原料为纯净物 ⑤只生成一种气体
(6)若用下图装置进行排空气法收集二氧化碳气体,则气体应从 (填b或c)口进入;

(7)下图是同学们在探究氧气性质实验中改进的实验装置图,简要回答甲、乙两个集气瓶中液体的作用 ,
。

| (1) | 长颈漏斗 |
| (2) | A-G |
2KClO3  2KCl+3 O2↑ 2KCl+3 O2↑ | |
| (3) | 能 |
| (4) | B |
| 试管口没有向下倾斜,导致反应中生成的水没有及时排出(或试管外壁有水、没有用外焰加热等) | |
| (5) | ③⑤ |
| (6) | b |
| (7) | 防止生成物熔化后溅落到集气瓶底部使集气瓶破裂 吸收燃烧产物,防止二氧化硫污染空气 |
分析:(1)熟练掌握化学常见的仪器的名称和用途;
(2)根据反应物状态与反应条件选择发生装置,根据生成气体的密度和溶解性选择收集装置.反应物为固体;
(3)D装置适合固液常温型的气体制取;
(4)根据氢气的可燃性及实验注意事项选择装置;试管破裂是由于试管局部冷热不均匀造成的;
(5)根据信息比较氧气、二氧化碳的共同点进行选择;
(6)根据二氧化碳的密度分析;
(7)甲中的水可以防止生成的四氧化三铁溅落炸裂瓶底;二氧化硫有毒,乙中的液体是氢氧化钠溶液,氢氧化钠溶液能吸收反应生成的二氧化硫气体.
解答:解:(1)a是长颈漏斗;
(2)氯酸钾和二氧化锰是固体,发生装置采用固固加热装置,排水法比排空气法收集纯净,故选择的组合是A G;反应的方程式为:2KClO3 2KCl+3 O2↑;
2KCl+3 O2↑;
(3)D装置适合固液常温型的气体制取,而氢气用锌粒和稀硫酸在常温下反应,故能,并且该装置还能控制反应的发生和停止;
(4)氢气还原氧化铜,实验步骤中要求先通氢气,防止爆炸,而这部分氢气没有参加反应,故需要排出,因此不能选A装置,而选择B装置;试管爆炸的原因可能有:试管口没有向下倾斜,导致反应中生成的水没有及时排出(或试管外壁有水、没有用外焰加热等);
(5)制取氧气可以采用过氧化氢溶液和稀盐酸反应,制取二氧化碳用石灰石和稀盐酸反应,经比较共同点是:③没有气体参加反应 ⑤只生成一种气体,这也是制取其他其他的共同点;
(6)因为二氧化碳的密度比空气大,故应该从长管(b)进,空气从短管排出;
(7)甲中的水可以防止生成的四氧化三铁溅落炸裂瓶底;因为二氧化硫有毒,乙中的液体是氢氧化钠溶液,氢氧化钠溶液能吸收反应生成的二氧化硫气体,防止污染空气.
故答案为:(1)长颈漏斗; (2)A、G;2KClO3 2KCl+3 O2↑; (3)能; (4)B;试管口没有向下倾斜,导致反应中生成的水没有及时排出(或试管外壁有水、没有用外焰加热等)
2KCl+3 O2↑; (3)能; (4)B;试管口没有向下倾斜,导致反应中生成的水没有及时排出(或试管外壁有水、没有用外焰加热等)
(5)③⑤; (6)b;(7)防止生成物熔化后溅落到集气瓶底部使集气瓶炸裂; 吸收燃烧产物,防止二氧化硫污染空气
(2)根据反应物状态与反应条件选择发生装置,根据生成气体的密度和溶解性选择收集装置.反应物为固体;
(3)D装置适合固液常温型的气体制取;
(4)根据氢气的可燃性及实验注意事项选择装置;试管破裂是由于试管局部冷热不均匀造成的;
(5)根据信息比较氧气、二氧化碳的共同点进行选择;
(6)根据二氧化碳的密度分析;
(7)甲中的水可以防止生成的四氧化三铁溅落炸裂瓶底;二氧化硫有毒,乙中的液体是氢氧化钠溶液,氢氧化钠溶液能吸收反应生成的二氧化硫气体.
解答:解:(1)a是长颈漏斗;
(2)氯酸钾和二氧化锰是固体,发生装置采用固固加热装置,排水法比排空气法收集纯净,故选择的组合是A G;反应的方程式为:2KClO3
 2KCl+3 O2↑;
2KCl+3 O2↑; (3)D装置适合固液常温型的气体制取,而氢气用锌粒和稀硫酸在常温下反应,故能,并且该装置还能控制反应的发生和停止;
(4)氢气还原氧化铜,实验步骤中要求先通氢气,防止爆炸,而这部分氢气没有参加反应,故需要排出,因此不能选A装置,而选择B装置;试管爆炸的原因可能有:试管口没有向下倾斜,导致反应中生成的水没有及时排出(或试管外壁有水、没有用外焰加热等);
(5)制取氧气可以采用过氧化氢溶液和稀盐酸反应,制取二氧化碳用石灰石和稀盐酸反应,经比较共同点是:③没有气体参加反应 ⑤只生成一种气体,这也是制取其他其他的共同点;
(6)因为二氧化碳的密度比空气大,故应该从长管(b)进,空气从短管排出;
(7)甲中的水可以防止生成的四氧化三铁溅落炸裂瓶底;因为二氧化硫有毒,乙中的液体是氢氧化钠溶液,氢氧化钠溶液能吸收反应生成的二氧化硫气体,防止污染空气.
故答案为:(1)长颈漏斗; (2)A、G;2KClO3
 2KCl+3 O2↑; (3)能; (4)B;试管口没有向下倾斜,导致反应中生成的水没有及时排出(或试管外壁有水、没有用外焰加热等)
2KCl+3 O2↑; (3)能; (4)B;试管口没有向下倾斜,导致反应中生成的水没有及时排出(或试管外壁有水、没有用外焰加热等)(5)③⑤; (6)b;(7)防止生成物熔化后溅落到集气瓶底部使集气瓶炸裂; 吸收燃烧产物,防止二氧化硫污染空气

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目