题目内容
地球是一颗蓝色的星球,表面大部分被海洋覆盖,海水中蕴含的元素多达80多种.同学们在学习过程中得知:工业上把海水晒制后得到的晶体称为粗盐,剩余的液体称为苦卤,小亮等同学对海水晒盐后的苦卤产生了浓厚的兴趣.
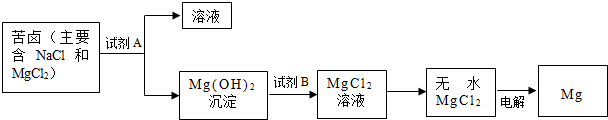
查阅资料得知:①苦卤中含有氯化镁、氯化钠、溴化钾、氯化钾等;②可以综合利用海水资源制备金属镁,如图是化工厂利用苦卤生产镁的流程,工业上为了使海水中的MgCl2完全反应,要加入过量的石灰乳.

(1)操作a的名称是
通电
(2)操作a后得到的溶液A的pH
(3)工业上冶炼镁常用电解MgCl2的方法,反应方程式为:MgCl2═Mg+
(4)写出第②、③两步反应的化学方程式:
②
查阅资料得知:①苦卤中含有氯化镁、氯化钠、溴化钾、氯化钾等;②可以综合利用海水资源制备金属镁,如图是化工厂利用苦卤生产镁的流程,工业上为了使海水中的MgCl2完全反应,要加入过量的石灰乳.

(1)操作a的名称是
过滤
过滤
,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、漏斗
漏斗
;通电
(2)操作a后得到的溶液A的pH
>
>
7(填“<、=、>”;(3)工业上冶炼镁常用电解MgCl2的方法,反应方程式为:MgCl2═Mg+
Cl2
Cl2
↑;(4)写出第②、③两步反应的化学方程式:
②
CaO+H2O═Ca(OH)2
CaO+H2O═Ca(OH)2
;③Mg(OH)2+2HCl═MgCl2+2H2O
Mg(OH)2+2HCl═MgCl2+2H2O
.分析:(1)根据生成物的成分和状态进行选择操作,可回忆实验室过滤操作的具体过程来完成本题,注意审题;
(2)根据过量的石灰乳来解答;
(3)根据反应原理及质量守恒定律来解答;
(4)根据反应原理及质量守恒定律来解答.
(2)根据过量的石灰乳来解答;
(3)根据反应原理及质量守恒定律来解答;
(4)根据反应原理及质量守恒定律来解答.
解答:解:(1)根据题意进过操作a后得到了氢氧化镁沉淀,所以操作是过滤.过滤用到的主要玻璃仪器有烧杯、漏斗和玻璃棒.
(2)由于所用的石灰乳是过量的,所以滤液中一定有氢氧化钙,所以溶液的pH>7;
(3)根据质量守恒定律可知生成物为Cl2,同时是在方程式中填空,必须保证方程式的准确性,所以必须标气体符号.
(4)反应②是氧化钙和水反应生成氢氧化钙,化学方程式:CaO+H2O═Ca(OH)2;
反应③是沉淀氢氧化镁和盐酸反应生成氯化镁和水,化学方程式:Mg(OH)2+2HCl═MgCl2+2H2O.
故答案为:(1)过滤;漏斗;
(2)>;
(3)Cl2;
(4)CaO+H2O═Ca(OH)2; Mg(OH)2+2HCl═MgCl2+2H2O.
(2)由于所用的石灰乳是过量的,所以滤液中一定有氢氧化钙,所以溶液的pH>7;
(3)根据质量守恒定律可知生成物为Cl2,同时是在方程式中填空,必须保证方程式的准确性,所以必须标气体符号.
(4)反应②是氧化钙和水反应生成氢氧化钙,化学方程式:CaO+H2O═Ca(OH)2;
反应③是沉淀氢氧化镁和盐酸反应生成氯化镁和水,化学方程式:Mg(OH)2+2HCl═MgCl2+2H2O.
故答案为:(1)过滤;漏斗;
(2)>;
(3)Cl2;
(4)CaO+H2O═Ca(OH)2; Mg(OH)2+2HCl═MgCl2+2H2O.
点评:本题难度不大,主要考查了学生对过滤操作的掌握和对书写化学方程式的技巧.

练习册系列答案
相关题目