题目内容
【题目】工上利用锌焙砂(主要成分是ZnO,还含有SiO2、Fe2O3、CuO等)生产碱式碳酸锌 [Zn2(OH)2CO3]的工艺流程如下:
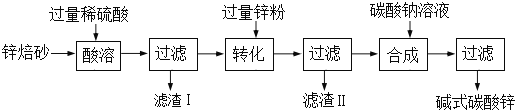
己知:①SiO2不溶于水也不与稀硫酸反应。② Fe2(SO4)3+Zn=2FeSO4+ZnSO4
请回答下列问题:
(1) “酸溶”过程中,Fe2O3发生的化学反应方程式为 _______________。
(2) “过滤”操作在实验室进行时,过滤器常由漏斗和_______________组成。
(3) “转化”时产生的少量气体是(写化学式,下同)________。滤渣Ⅱ的成分为_______________。
(4)“合成”过程中同时生CO2和Na2SO4,请写出合成过程的反应方程式______
【答案】Fe2O3+3H2SO4==Fe2(SO4)3+3H2O 滤纸 H2 Zn、Fe、Cu 2Na2CO3+2ZnSO4 +H2O == Zn2(OH)2CO3↓+CO2↑+2Na2SO4
【解析】
(1)“酸溶”过程中,Fe2O3发生的化学反应是氧化铁和硫酸反应生成硫酸铁和水,对应的化学方程式为 Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(2)“过滤”操作在实验室进行时,过滤器常由漏斗和滤纸组成;
(3)由于加入的硫酸过量,所以“转化”时是硫酸和锌反应生成了氢气,所以产生的少量气体的化学式为 H2;由于锌过量,所以导致硫酸铁转化为硫酸亚铁进而继续转化为铁,而硫酸铜被锌转化为铜,还有过量的锌,所以滤渣Ⅱ的成分为 Zn、Fe、Cu;
(4)“合成”过程中硫酸锌和碳酸钠是反应物,由于生成Zn2(OH)2CO3同时生CO2和Na2SO4,由于生成物含有氢元素,所以根据质量守恒定律以及反应环境,可知水也是反应物,所以合成过程的反应方程式 2Na2CO3+2ZnSO4+H2O═Zn2(OH)2CO3↓+CO2↑+2Na2SO4。

 阅读快车系列答案
阅读快车系列答案【题目】目前人类发现的元素共有一百多种,其中非金属元素22种,其余为金属元素。这一百多种元素组成了几千万种物质。下表是地壳、人体和海水中含量较高的一些元素,请依据这些元素回答下列问题。
元素名称 | 氢 | 碳 | 氧 | 氯 | 钠 | 铁 |
元素符号 | H | C | O | Cl | Na | Fe |
(1)某固体单质在氧气中燃烧火星四射,生成黑色固体。写出该反应的化学方程式________。
(2)若某固体单质在完全燃烧和不完全燃烧时,生成不同的气体,该固体不完全燃烧时反应的化学程式为__________。
(3)若某可燃性气体由两种元素组成,该气体一定含有的元素是_______,可能含有的元素是_______。
(4)若X和Y反应生成两种维持人体正常生理活动所必需的物质。向X溶液中滴加2~3滴无色酚酞试液,溶液变红;再滴加Y溶液至溶液无色。则X是______(填化学式,下同),Y是_________。
(5)若某元素的单质A及其氧化物B均与D溶液反应,分别生成该元素的化合物E和F,且这种元素在B和F中的化合价相同。B与D反应的化学方程式为__________;
(6)工业上炼得的某种钢材,测得其含碳量为0.6%(杂质元素不考虑),若碳元素主要以Fe2C和Fe3C的形式存在,则该钢样品中Fe2C和Fe3C的质量分数(ω)范围是_________。
A 0.03%<ω<2% B 0.6%<ω<0.87%
C 2.48%<ω<3.6% D 6.2%<ω< 9%
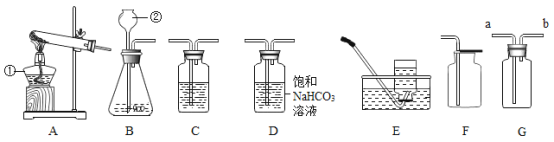
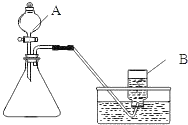
【题目】双氧水(H2O2)不仅可以用于美容业中除去色斑,也可以在常温下以二氧化锰为催化剂发生分解反应制取氧气.某同学设计了如图装置制取下表中的三种纯净、干燥的气体.
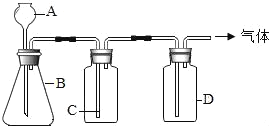
(A、B、C、D表示相应仪器中加入的试剂)
气体 | A | B | C | D |
O2 | 双氧水溶液 | 二氧化锰 | 水 | 氢氧化钠固体 |
H2 | 稀硫酸 | 铜 | 氢氧化钠溶液 | 浓硫酸 |
CO2 | 稀盐酸 | 大理石 | 氢氧化钠溶液 | 浓硫酸 |
①上述方法中可以得到的纯净、干燥的气体是_____(填化学式),装置D中所用药品还可以用_____代替.
②指出不能用上述方法得到的气体,并说明理由.(任选一种)气体_____,理由是_____.