题目内容
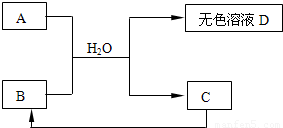 下列A~D为初中化学常见物质,其中A为含有金属钠离子的盐,C为大理石的主要成分.它们之间存在下列关系:
下列A~D为初中化学常见物质,其中A为含有金属钠离子的盐,C为大理石的主要成分.它们之间存在下列关系:(1)A的化学式 ;C的化学式 .
(2)D中一定含有的溶质是 .用化学方程式表示你判断的理由:
① ;
② .
(3)D还可能含有的溶质是 .
【答案】分析:根据C是大理石的主要成分,所以C就是碳酸钙,A为钠盐且和B在水中反应生成碳酸钙,所以A为碳酸钠;碳酸钙高温会生成氧化钙和二氧化碳,所以B为氧化钙.
解答:解:(1)C是大理石的主要成分,所以C就是碳酸钙,A为钠盐且和B在水中反应生成碳酸钙,所以A为碳酸钠;
(2)碳酸钙高温会生成氧化钙和二氧化碳,所以B为氧化钙;
氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,所以D中一定含有氢氧化钠,发生反应的化学方程式为:CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)若氢氧化钙过量,则无色溶液D中还含有氢氧化钙;若碳酸钠过量,则无色溶液D中还含有碳酸钠.
故答案为:(1)Na2CO3,CaCO3;
(2)NaOH;CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)Ca(OH)2 或Na2CO3.
点评:该题为框图式物质推断题,完成此类题目的关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.
解答:解:(1)C是大理石的主要成分,所以C就是碳酸钙,A为钠盐且和B在水中反应生成碳酸钙,所以A为碳酸钠;
(2)碳酸钙高温会生成氧化钙和二氧化碳,所以B为氧化钙;
氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,所以D中一定含有氢氧化钠,发生反应的化学方程式为:CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)若氢氧化钙过量,则无色溶液D中还含有氢氧化钙;若碳酸钠过量,则无色溶液D中还含有碳酸钠.
故答案为:(1)Na2CO3,CaCO3;
(2)NaOH;CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)Ca(OH)2 或Na2CO3.
点评:该题为框图式物质推断题,完成此类题目的关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.

练习册系列答案
相关题目
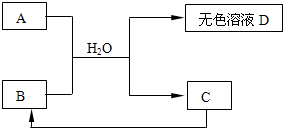 下列A~D为初中化学常见物质,其中A为含有金属钠离子的盐,C为大理石的主要成分.它们之间存在下列关系:
下列A~D为初中化学常见物质,其中A为含有金属钠离子的盐,C为大理石的主要成分.它们之间存在下列关系: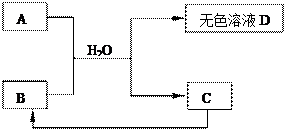
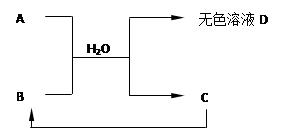

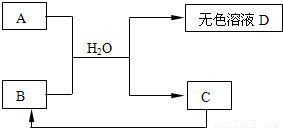 下列A~D为初中化学常见物质,其中A为含有金属钠离子的盐,C为大理石的主要成分.它们之间存在下列关系:
下列A~D为初中化学常见物质,其中A为含有金属钠离子的盐,C为大理石的主要成分.它们之间存在下列关系: