题目内容
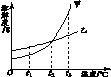
右图是NaCl、MgSO4的溶解度曲线。请回答下列问题:
加热t2℃的MgSO4饱和溶液,会看到的现象是 ;
将t1℃时MgSO4的饱和溶液升温至t3℃,溶质质量分数的变化是___________(填“变大”、“变小”或“不变”);

在t3℃时,将NaCl的不饱和溶液恒温蒸发100g水后,析出ag固体,若再继续恒温蒸发100g水,则析出固体的质量________ag(填“>”、“<”或“=”);
若要将t2℃的MgSO4饱和溶液150g稀释至10%,需加水___________g。
加热t2℃的MgSO4饱和溶液,会看到的现象是 ;
将t1℃时MgSO4的饱和溶液升温至t3℃,溶质质量分数的变化是___________(填“变大”、“变小”或“不变”);

在t3℃时,将NaCl的不饱和溶液恒温蒸发100g水后,析出ag固体,若再继续恒温蒸发100g水,则析出固体的质量________ag(填“>”、“<”或“=”);
若要将t2℃的MgSO4饱和溶液150g稀释至10%,需加水___________g。
(1) 有固体析出 (2) 不变 (3) > (4) 350
试题分析:(1)根据溶解度曲线可知,当温度大于t2℃时,MgSO4的溶解度随温度的升高而减小,故加热t2℃的MgSO4饱和溶液会有溶质MgSO4的析出,故可见有固体析出的现象。
(2)根据溶解度曲线可知,从t1℃升温至t3℃时,MgSO4的溶解度会先变大后变小,但最终t3℃时MgSO4的溶解度>t1℃时MgSO4的溶解度,故将t1℃时MgSO4的饱和溶液升温至t3℃时,溶液会变成不饱和溶液,由于此过程中,溶质、溶剂的质量均未变,故溶质质量分数不变。
(3)由于第一次蒸发时的溶液是不饱和溶液,故蒸发时需要先蒸发掉部分的水,使溶液变为饱和溶液(此时未有晶体析出),然后再继续蒸发,才有ag晶体析出,即相当于在t3℃时,将NaCl的饱和溶液恒温蒸发<100g的水后,析出ag固体;所以,若对该饱和溶液再继续恒温蒸发100g水,则析出固体的质量>ag。
(4)根据溶解度曲线可知,t2℃时MgSO4的溶解度是50g,根据饱和溶液的溶质质量分数=
 ×100﹪可知,t2℃的MgSO4饱和溶液的溶质质量分数=
×100﹪可知,t2℃的MgSO4饱和溶液的溶质质量分数= ×100﹪=33.3%;又因为稀释的过程中,改变的是溶剂的质量,而溶质的质量不变,故可设需加水的质量为xg,则有150g×33.3%=(150g+x)×10﹪,解得x=350g。
×100﹪=33.3%;又因为稀释的过程中,改变的是溶剂的质量,而溶质的质量不变,故可设需加水的质量为xg,则有150g×33.3%=(150g+x)×10﹪,解得x=350g。点评:本题主要考查了固体溶解度曲线所表示的意义,及根据固体溶解度曲线来解决相关问题,注重培养学生的分析问题、解决问题的能力,解题的关键是要熟记和理解固体溶解度曲线及其应用,以及溶质质量分数的有关计算。

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目