题目内容
【题目】用化学用语填空
(1)碳酸钠的化学式为_________;
(2)硝酸铵中的阴离子是_________;
(3)人体中含量最多的金属元素是______;
(4)镁离子____________;
(5)硫化钠中硫的化合价__________;
(6)氧化铁的化学式为_______________。
【答案】Na2CO3 NO3- Ca Mg2+ ![]() Fe2O3
Fe2O3
【解析】
(1)碳酸钠中钠元素显+1价,碳酸根显-2价,根据化合物中各元素的化合价为零可知,其化学式为:Na2CO3;
(2)硝酸铵中的阴离子是硝酸根离子,离子符号为:NO3-;
(3)人体中含量最多的金属元素是钙元素,元素符号为:Ca;
(4)离子的表示方法是在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,。在其元素符号前加上相应的数字,镁离子的符号为Mg2+;
(5)硫化钠中钠元素化合价为+1价,根据化合物中各元素的化合价为零可知,硫的化合价为-2;化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,硫化钠中硫的化合价表示为:![]() ;
;
(6)氧化铁中氧元素化合价为-2价,铁元素化合价为+3价,根据化合物中各元素的化合价为零可知,其化学式为Fe2O3。

【题目】钙片的标签如图所示,且知此钙片成分中只有碳酸钙中含有钙元素,此标签中的含钙量是否正确?
(1)______(填“正确”或“错误”),为测定其含钙量,小东每次取10片钙片放入已称量的含足量稀盐酸的烧杯中,充分反应后再称取烧杯和剩余物的总质量,小东做了三次实验数据如下:
物质的质量 | 第1次 | 第2次 | 第3次 | 平均值 |
反应前:烧杯+稀盐酸 | 22g | 22g | 22g | 22g |
10片钙片 | 8g | 8g | 8g | 8g |
反应后:烧杯+稀盐酸 | 26.7g | 26.5g | 26.9g | 26.7g |
(2)每片钙片中含碳酸钙质量是____g
(3)通过小东的实验,你建议厂家如何修改标签?______。

【题目】化学是造福人类的科学,请利用所学知识回答下列问题。
(1)新型材料有着广泛的应用。
应用 | “蛟龙”号深潜器 | “神舟”五号宇航员航天服 | 新型水处理剂 |
用到的材料 | 特种钢 | 高强度涤纶 | 纳米铁粉 |
①上述材料中属于有机合成材料的是______。
②纳米铁粉能吸附废水中的某些污染物,被吸附后的废水经沉降、过滤可去除污染物。
下列物质也能因吸附而具有净水作用的是______(填字母)
a.生石灰 b.活性炭 c.纯碱
(2)溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。
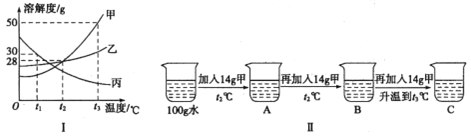
①t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______。
②某同学按图Ⅱ所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是______(填字母)。
③t3℃时向盛有40g甲物质的烧杯中加入50g水充分溶解后,所得溶液溶质的质量分数为______。(结果精确到0.1%)
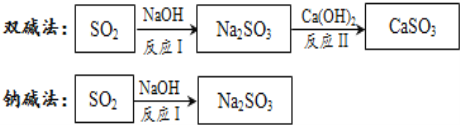
【题目】工业烟气通常含二氧化硫,在排放前需经脱硫处理![]() 如图是两种常用脱硫工艺中含硫物质的转化路径
如图是两种常用脱硫工艺中含硫物质的转化路径![]() 部分产物已略
部分产物已略![]() .
.
(1)下列环境问题与![]() 有关的是 ______
有关的是 ______ ![]() 填字母序号
填字母序号![]() .
.
A酸雨 B温室效应 C臭氧空洞
(2)双碱法中的“双碱”指的是 ______![]() 填化学式
填化学式![]() .
.
(3)写出反应Ⅰ的化学方程式: ______ .
(4)反应Ⅱ所属的基本反应类型是 ______ .
(5)已知部分原料的价格如下表所示.
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.90 |
两种工艺中,处理相同量的SO2,双碱法所需的原料成本更低,原因是______![]() 物质组成和变化分析
物质组成和变化分析![]() .
.