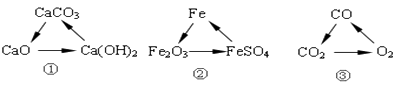
题目内容
【题目】为减少污染并变废为宝,某化学小组在实验室探究工业废水的综合利用,设计了以下流程图并完成了回收铜和硫酸锌的实验.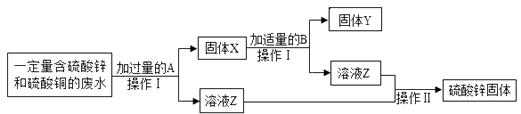
(1)操作Ⅰ的名称是 , 操作Ⅱ中玻璃棒的作用是;
(2)X的成分为;
(3)加入B时反应的化学方程式为;
(4)理论上所得硫酸锌晶体的质量(填“>”“<”或“=”)原废液中硫酸锌的质量.
【答案】
(1)过滤;防止液滴飞溅
(2)锌、铜
(3)Zn+H2SO4=ZnSO4+H2↑
(4)>
【解析】根据所学知识和题中信息知,(1)操作Ⅰ的名称是过滤。操作Ⅱ中玻璃棒的作用是防止液滴飞溅。(2)X的成分为锌、铜。(3)加入B时反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑。(4)理论上所得硫酸锌晶体的质量>原废液中硫酸锌的质量.
故答案为:(1)过滤;防止液滴飞溅;(2)锌、铜;(3)Zn+H2SO4=ZnSO4+H2↑;(4)>(1)根据操作名称和作用可以解答
(2)根据试验流程可知,这个试验是回收铜和硫酸锌的试验
(3)锌可以和硫酸铜反应,但过量的锌仍然是杂质
(4)根据流程图可知反应过程中有硫酸锌生成

 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案【题目】在学习盐酸的化学性质时,小红、芳芳两位同学分别作了碳酸钠溶液和稀盐酸反应的实验如图所示。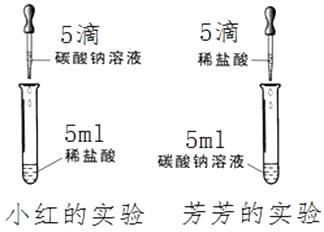
(1)【实验现象】小红在实验中观察到有气泡冒出,而芳芳所做的实验无现象。写出小红实验的化学反应方程式 :。
(2)【实验讨论】芳芳同学的试验为什么观察不到有气泡?
反应后溶液的溶质有哪些?
【查阅资料】①碳酸钠和稀盐酸反应生成物受到盐酸的质
量影响,稀盐酸过量生成二氧化碳,若盐酸量不足则生成碳酸氢钠;②碳酸氢钠与氯化钙溶液混合不发生反应,而碳酸钠和氯化钙溶液反应生成沉淀,且碳酸钠和碳酸氢钠溶液都呈碱性,氯化钙溶液呈中性。
【猜想与假设】实验反应后溶液中溶质可能有:①NaHCO3、NaCl、Na2CO3; ②NaHCO3、NaCl;
③NaHCO3、NaCl、HCl。
芳芳同学认为猜想③肯定不成立,理由是。
(3)【实验设计】确定芳芳同学实验是否生成碳酸氢钠,并证明反应后的产物。
实验步骤 | 实验现象 | 实验结论 |
A、取上述溶液少量于试管中,加 | 产生白色沉淀 | 猜想①正确 |
B、取步骤A所得上层清液少量,滴加 溶液。 |
(4)【实验反思】若用少量的稀盐酸鉴定氢氧化钠是否变质,发现无气泡冒出,则证明氢氧化钠溶液没有变质。对此实验结论,你是否赞同?若不赞同,还需说明理由。。