题目内容
某同学在实验室用氯酸钾和二氧化锰混合物制取氧气.已知氯酸钾、二氧化锰的混合物为26g,加热后完全反应,最后生物物质的质量为16.4g.求:
(1)生成氧气的质量为 g.
(2)原混合物中二氧化锰的质量是多少?
(3)原混合物中氯酸钾的质量分数是多少?
(1)生成氧气的质量为
(2)原混合物中二氧化锰的质量是多少?
(3)原混合物中氯酸钾的质量分数是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据质量守恒定律可以计算出反应生成氧气的质量;
(2)二氧化锰在该反应中充当了催化剂,根据催化剂的定义可以知道,在 反应前后二氧化锰的质量没有改变,所以可以根据化学方程式计算出氯酸钾的质量,然后求出二氧化锰的质量即可;
(3)根据(2)中求算的氯酸钾的质量,求出原混合物中氯酸钾的质量分数即可.
(2)二氧化锰在该反应中充当了催化剂,根据催化剂的定义可以知道,在 反应前后二氧化锰的质量没有改变,所以可以根据化学方程式计算出氯酸钾的质量,然后求出二氧化锰的质量即可;
(3)根据(2)中求算的氯酸钾的质量,求出原混合物中氯酸钾的质量分数即可.
解答:解:(1)根据质量守恒定律可以知道生成氧气的质量为:26g-16.4g=9.6g;
(2)设氯酸钾的质量为x
2KClO3
2KCl+3O2↑
245 96
x 9.6g
=
解得:x=24.5g
所以原混合物中二氧化锰的质量为:26g-24.5g=1.5g;
(3)原混合物中氯酸钾的质量分数为
×100%=94.2%
答:(1)生成氧气的质量为9.6g;
(2)原混合物中二氧化锰的质量为1.5g;
(3)原混合物中氯酸钾的质量分数为94.2%.
(2)设氯酸钾的质量为x
2KClO3
| ||
| △ |
245 96
x 9.6g
| 245 |
| 96 |
| x |
| 9.6g |
解得:x=24.5g
所以原混合物中二氧化锰的质量为:26g-24.5g=1.5g;
(3)原混合物中氯酸钾的质量分数为
| 24.5g |
| 26g |
答:(1)生成氧气的质量为9.6g;
(2)原混合物中二氧化锰的质量为1.5g;
(3)原混合物中氯酸钾的质量分数为94.2%.
点评:根据质量守恒定律,由反应前后固体物质质量差即反应所产生氧气的质量;利用二氧化锰为反应的催化剂,反应前后质量不变,由混合物质量与参加反应的氯酸钾质量差可求得二氧化锰的质量.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
资源是宝贵的财富,下列有关资源的说法不正确的是( )
| A、空气是一种宝贵的能源 |
| B、地球上的生物种类千差万别,但体内水的质量一般都在60%以上 |
| C、海洋是巨大的资源宝库,其中含有100多种元素 |
| D、金属资源都是以化合物形式存在于地壳和浩瀚的海洋中 |
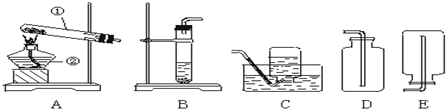
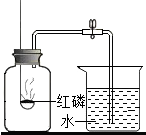 为测定空气中氧气的含量,甲、乙两同学用如图所示的装置分别进行了实验探究.
为测定空气中氧气的含量,甲、乙两同学用如图所示的装置分别进行了实验探究.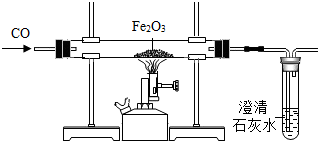 铜、铁、铝是人类广泛使用的金属,它们与我们的生活息息相关.
铜、铁、铝是人类广泛使用的金属,它们与我们的生活息息相关.