题目内容
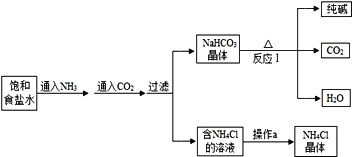
【题目】我国著名化学家侯德榜先生发明的“侯氏制碱法”,因原料利用率高,能进行连续生产,从而享誉中外,如图为侯氏制碱法的基本流程示意图,回答问题。
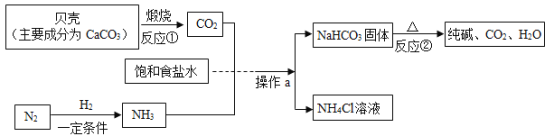
(1)操作a的名称是___________________________。
(2)反应②中的化学方程式为___________________________,其基本反应类型为___________________________。
(3)仔细观察流程图,其中可循环利用的物质是___________________________。
(4)化学肥料对农作物生长具有促进作用,得到的副产品NH4Cl属于___________________________(填字母)。
A 氮肥
B 磷肥
C 钾肥
D 复合肥
(5)该方法制出的纯碱固体中常含有NaCl,检验该固体中是否含有NaCl的方法是___________________________。
附:部分碱、酸、盐的溶解性表(20°C)
| OH- | NO3- | Cl- | CO32- |
H+ | 溶、挥 | 溶、挥 | 溶、挥 | |
Na+ | 溶 | 溶 | 溶 | 溶 |
Ag+ | 一 | 溶 | 不 | 不 |
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“挥”表示挥发性,“一”表示那种物质不存在或遇到水就分解了。
【答案】过滤 ![]() 分解反应 二氧化碳(或CO2) A 取样品少许于一支试管中,加入过量稀硝酸至不再产生气泡为止,再加入硝酸银溶液,若有白色沉淀产生,说明样品中含有NaCl,反之,则样品中无NaCl(其他合理答案均可)
分解反应 二氧化碳(或CO2) A 取样品少许于一支试管中,加入过量稀硝酸至不再产生气泡为止,再加入硝酸银溶液,若有白色沉淀产生,说明样品中含有NaCl,反之,则样品中无NaCl(其他合理答案均可)
【解析】
(1)操作A得到碳酸氢钠固体和氯化铵溶液,所以该操作是过滤;
(2) 反应②是碳酸氢钠受热分解为碳酸钠、二氧化碳和水,高于分解反应,化学方程式为![]() ;
;
(3)由流程图可知,二氧化碳既是反应物又是生成物,其中可循环利用的物质是二氧化碳;
(4)氯化铵中只含有植物生长所需的氮元素,故氯化铵属于氮肥;
(5) 氯化钠与硝酸银溶液反应可生成氯化银白色沉淀,碳酸钠与硝酸银溶液反应也可生成白色沉淀,故应排除CO32-的干扰,因此检验纯碱固体中含有氯化钠的方法可以是取该纯碱样品少许于一支试管中,加入过量稀硝酸至不再产生气泡为止,再加入硝酸银溶液,若有白色沉淀产生,说明样品中含有NaCl,反之,则样品中无NaCl。

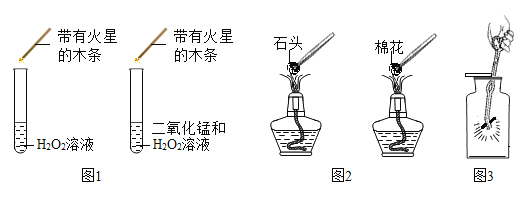
【题目】某研究性学习小组在进行“利用燃碳法测定空气中氧气的休积分数”的实验时(装置如图甲所示),发现一个现象:氢氧化钠溶液(易吸收二氧化碳而不吸收一 氧化碳) 吸收生成的二氧化碳后,进入集气瓶中水的体积分数仍然小于1/5。
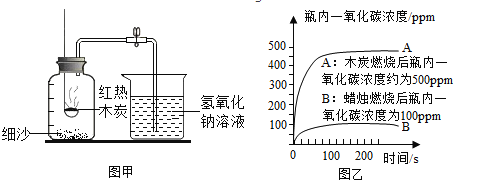
(1)教材中利用燃烧红磷法测定空气中氧气的体积分数,选择该药品的原因是:_________________、________________。
(2)[提出问题]测量不准确的原因是什么呢?
[猜想与假设]他们分别作出如下猜想:
甲同学:可能是木炭的量过少;
乙同学:可能是木炭足量,但其燃烧没有消耗完集气瓶中的氧气;
丙同学:可能是木炭燃烧生成了一氧化碳。
小组同学发现实验结束后,燃烧匙中还残留有黑色固体,因此他们都认为甲同学的猜想不合理。
[查阅资料]木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数分别高达 14. 0%、8. 0%和16. 0%。
乙同学根据如图所示装置设计了如下实验,请你填写下表:
实验步骤 | 实验现象 | 实验结论 |
将足量木炭点燃,迅速插入集气瓶中 | 木炭先继续燃烧,一段时间后熄灭 | 木炭燃烧没有消耗完集气瓶中的氧气 |
待集气瓶冷却后,将燃着的____________,(填“棉花”或“蜡烛”)再伸入该集气瓶中 | _______________。 |
[交流与反思]请写出木炭不完全燃烧的化学方程式:________________。
(3)木炭熄灭后,乙同学选择可燃物的依据是_____________________。
(4)丙同学使用一氧化碳浓度传感器测得木炭、蜡烛分别在密闭集气瓶里燃烧停止后瓶内一氧化碳的浓度变化曲线如乙图。根据此曲线图分析用上述装置不能准确测出氧气体积分数的原因___________________。
(5)在实际实验过程中,有部分燃碳法实验测定的空气中氧气的体积分数可以达到20%,推测造成这一现象的原因:__________________。
【题目】CO2通人NaOH溶液中无明显现象,为探究两者是否发生反应,某兴趣小组尝试用不同的方法进行实验。
(1)实验一:小雨取一充满CO2的矿泉水瓶, 加入一定量的水,立即拧紧瓶盖, 振荡,发现瓶子变瘪。小雨另取一相同的充满CO2的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X。可观察到加人NaOH溶液的瓶子变瘪程度更大,证明_____。
(2)实验二:检验溶液X的成分。小亮首先对溶液中溶质的成分进行了猜想。
[提出猜想]①只含有Na2CO3 ②只 含有NaOH ③含有 NaOH和Na2CO3
[进行实验]小亮取少量溶液X于一支洁净的试管中,然后向其中滴加几滴无色酚酞溶液,溶液变成红色,于是小亮得出结论,猜想①一定不成立。而小明认为小亮的结论不正确,小明的理由是_____。
小明设计了如下表所示的实验方案,最终准确检验出溶液X的成分,请帮忙完成表格。
实验步骤 | 实验现象及方程式 | 实验结论 |
a.取适量溶液X于一支洁净的试管中,加人过量的_____溶液 | 有 白色沉淀产生,化学方程式为_____。 | 猜想_____不成立 |
b.取步骤a得到的上层清液于另一支洁净的试管中,滴加几滴无色酚酞溶液 | _____。 | 猜想①成立 |
(3)实验三:小强将CO2持续通人一定浓度的NaOH溶液中,然后按照小明的方案检验反应后溶液中的溶质成分,结果没有看到白色沉淀产生。小强联想起教材中的一个反应: ![]() ,于是得出氢氧化钠溶液中通人过量CO2,反应后生成_____(填化学式),因此在实验中没有产生白色沉淀。
,于是得出氢氧化钠溶液中通人过量CO2,反应后生成_____(填化学式),因此在实验中没有产生白色沉淀。