题目内容
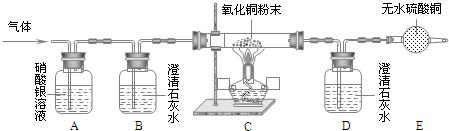
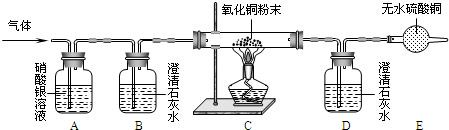
某气体可能由H2、CO、CO2、HCl中的一种或几种组成,为确定其成分,进行上述实验,气体通过有关装置时观察的现象如下,请根据题意回答问题:(假设反应均完全)

①判断该气体中一定含有
②气体中可能含有
③判断该气体中可能含有

| 装置编号 | A | B | C | D | E |
| 试剂 | 硝酸银溶液 | 澄清石灰水 | 氧化铜粉末 | 澄清石灰水 | 无水硫酸铜 |
| 现象 | 无明显现象 | 变浑浊 | 黑色变红色 | 变浑浊 | 变蓝色 |
CO2和CO
CO2和CO
;②气体中可能含有
氢气
氢气
;理由是E处无水硫酸铜变蓝色,说明有水,但水不一定来自混合气还原氧化铜得到的,可能来自于澄清石灰水或来自于空气;
E处无水硫酸铜变蓝色,说明有水,但水不一定来自混合气还原氧化铜得到的,可能来自于澄清石灰水或来自于空气;
;③判断该气体中可能含有
氢气
氢气
;若想证明该气体是否存在应如何改进装置在B、C之间加一个浓硫酸的洗气装置,再将E处无水硫酸铜移到D装置的前面
在B、C之间加一个浓硫酸的洗气装置,再将E处无水硫酸铜移到D装置的前面
.分析:根据所看到的现象分析出原因,推出结论.氯离子会与银离子生成沉淀,二氧化碳会使澄清石灰水变浑浊,氢气和一氧化碳具有还原性,水会使无水硫酸铜变蓝进行分析判断;混合气通过A(硝酸银溶液)无明显现象,说明了一定无氯化氢,会使B处澄清石灰水变浑浊,说明了一定存在二氧化碳;D处澄清石灰水变浑浊,说明物质与氧化铜反应生成了二氧化碳,所以混合气中含有一氧化碳;C处氧化铜粉末变红色,说明有还原性气体即氢气或一氧化碳;E处无水硫酸铜变蓝色,说明有水,但水不一定来自混合气.
解答:解:①混合气通过A(硝酸银溶液)无明显现象,说明了一定无氯化氢;B处石灰水变浑浊,说明混合气中一定有二氧化碳;一氧化碳能还原氧化铜生成二氧化碳,B处石灰水已经把原来的二氧化碳除掉,D处石灰水又变浑浊,说明C反应中有二氧化碳生成,所以混合气中一定有一氧化碳;
②C处氧化铜粉末变红色,说明有还原性气体即氢气或一氧化碳,上边已经证明含有一氧化碳,氢气可能有可能没有,E处无水硫酸铜变蓝色,说明有水,但水不一定来自混合气还原氧化铜得到的,可能来自于澄清石灰水或来自于空气;所以混合气体中可能含有氢气;
③由于氢气还原氧化铜生成铜和水,证明有水生成,首先通过氧化铜之前把原来的水除掉,在B、C之间加一个浓硫酸的洗气装置,再将E处无水硫酸铜移到D装置的前面,就能说明是否有水生成了,无水硫酸铜变蓝色,说明有水,说明含有氢气,无水硫酸铜不变蓝色,说明没有水生成,没有氢气.
故答案为:
①CO2和CO;
②氢气;E处无水硫酸铜变蓝色,说明有水,但水不一定来自混合气还原氧化铜得到的,可能来自于澄清石灰水或来自于空气;
③氢气;在B、C之间加一个浓硫酸的洗气装置,再将E处无水硫酸铜移到D装置的前面.
②C处氧化铜粉末变红色,说明有还原性气体即氢气或一氧化碳,上边已经证明含有一氧化碳,氢气可能有可能没有,E处无水硫酸铜变蓝色,说明有水,但水不一定来自混合气还原氧化铜得到的,可能来自于澄清石灰水或来自于空气;所以混合气体中可能含有氢气;
③由于氢气还原氧化铜生成铜和水,证明有水生成,首先通过氧化铜之前把原来的水除掉,在B、C之间加一个浓硫酸的洗气装置,再将E处无水硫酸铜移到D装置的前面,就能说明是否有水生成了,无水硫酸铜变蓝色,说明有水,说明含有氢气,无水硫酸铜不变蓝色,说明没有水生成,没有氢气.
故答案为:
①CO2和CO;
②氢气;E处无水硫酸铜变蓝色,说明有水,但水不一定来自混合气还原氧化铜得到的,可能来自于澄清石灰水或来自于空气;
③氢气;在B、C之间加一个浓硫酸的洗气装置,再将E处无水硫酸铜移到D装置的前面.
点评:在解此类题时,首先根据题中的现象推出存在或不存在的物质,检验氯化氢气体是否存在用硝酸银溶液,检验二氧化碳用澄清石灰水,检验一氧化碳时先通过灼热的氧化铜,再通过澄清石灰水,检验氢气时先通过灼热的氧化铜,再通过无水硫酸铜.

练习册系列答案
相关题目
某气体可能由H2、HCl、CO2、H2O、CO中的一种或几种组成,为确定其成分,进行如下实验: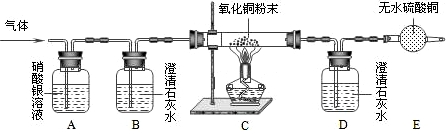
气体通过有关装置时所观察到的现象如下:
试推断:
(1)该气体中一定没有 ;
(2)该气体中一定含有 ;
(3)该气体中可能含有 ;
(4)写出C装置中发生反应的化学方程式 .

气体通过有关装置时所观察到的现象如下:
| 装置编号 | A | B | C | D | E |
| 试剂 | AgNO3溶液 | 澄清石灰水 | CuO粉末 | 澄清石灰水 | 无水CuSO4 |
| 现象 | 无明显变化 | 变浑浊 | 变红色 | 无明显变化 | 变蓝色 |
(1)该气体中一定没有
(2)该气体中一定含有
(3)该气体中可能含有
(4)写出C装置中发生反应的化学方程式
某气体可能由H2、CO、CO2、H2O、HCl中的一种或几种组成,为确定其成分,进行如下实验:(友情提示:无水硫酸铜遇水会变成蓝色)
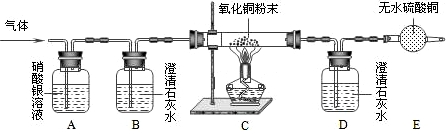
气体通过有关装置时观察到的现象如下:
| 装置编号 | A | B | C | D | E |
| 试 剂 | 硝酸银溶液 | 澄清石灰水 | 氧化铜粉末 | 澄清石灰水 | 无水硫酸铜 |
| 现 象 | 无明显变化 | 变浑浊 | 变红色 | 无明显变化 | 变蓝色 |
(1)该气体中一定含有______,一定没有______.
(2)若要证明可能存在的物质,应在______位置(填选项)增加某一装置来检验.
A、在A装置前 B、在A、B之间 C、在B、C之间 D、在C、D之间
(3)请写出D中所发生反应的化学方程式:______.