题目内容
如图是某品牌补铁剂的标签。请回答:

(1)富马酸亚铁中C、H、Fe、O原子个数比为 。
(2)富马酸亚铁中各种元素的质量比为 。
(3)若每次服用1包该补铁剂,计算摄入铁元素的质量为多少毫克(计算结果取整数)。

(1)富马酸亚铁中C、H、Fe、O原子个数比为 。
(2)富马酸亚铁中各种元素的质量比为 。
(3)若每次服用1包该补铁剂,计算摄入铁元素的质量为多少毫克(计算结果取整数)。
(1)4∶2∶1∶4
(2)C∶H∶Fe∶O=24∶1∶28∶32
(3)0.2g×56÷(12×4+1×2+56+16×4) ×1000 mg/ g=60mg
(2)C∶H∶Fe∶O=24∶1∶28∶32
(3)0.2g×56÷(12×4+1×2+56+16×4) ×1000 mg/ g=60mg
分析:(1)根据分子式判读即可.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据题意、结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解:(1)根据分子式,富马酸亚铁中C、H、Fe、O原子个数比为4:2:1:4.
(2)富马酸亚铁中碳、氢、铁、氧四种元素的质量比为(12×4):(1×2):(56×1):(16×4)=24:1:28:32.
(3)根据题意,每包含富马酸亚铁0.2g,每次服用2包该补铁剂,则每次服用的补铁剂中含富马酸亚铁的质量为0.2g×2=0.4g,
其中含铁元素的质量为0.4g×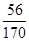 ×100%=0.132g=132mg.
×100%=0.132g=132mg.
故答案为:(1)4:2:1:4;(2)24:1:28:32;(3)132.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据题意、结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解:(1)根据分子式,富马酸亚铁中C、H、Fe、O原子个数比为4:2:1:4.
(2)富马酸亚铁中碳、氢、铁、氧四种元素的质量比为(12×4):(1×2):(56×1):(16×4)=24:1:28:32.
(3)根据题意,每包含富马酸亚铁0.2g,每次服用2包该补铁剂,则每次服用的补铁剂中含富马酸亚铁的质量为0.2g×2=0.4g,
其中含铁元素的质量为0.4g×
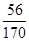 ×100%=0.132g=132mg.
×100%=0.132g=132mg.故答案为:(1)4:2:1:4;(2)24:1:28:32;(3)132.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目