题目内容
(2011?江西模拟)实验室现需要6.72L纯净的氧气(在标准状况下,氧气的密度是1.429g/L).某同学用质量比为3:1的氯酸钾和二氧化锰制取氧气,并回收二氧化锰.下表为该同学实验的有关数据:| 实验收集6.72L氧气后, 试管内固体剩余物的质量 | 充分加热后试管内 固体剩余物的质量 |
| 39.4g | 34.6g |
(2)最多能回收到多少克二氧化锰?
【答案】分析:(1)该同学总共收集到氧气的质量为第一次收集的6.72L氧气的质量与之后充分加热后第二次所收集氧气的质量总和,利用质量守恒定律,由充分加热前后试管内固体物质的质量差可计算出第二次所收集氧气的质量,第一次所收集氧气的质量可利用m=ρV进行计算;
(2)利用反应的化学方程式,由二次所收集氧气的总质量计算出所加氯酸钾的质量,根据用质量比为3:1的氯酸钾和二氧化锰制取氧气,求出加入的二氧化锰的质量;根据二氧化碳是催化剂剂在反应前后质量不变,收集到的二氧化锰的质量即所加入二氧化锰的质量.
解答:解:(1)第一次收集到氧气的质量:6.72L×1.429g/L=9.6g
第二次(充分加热)收集到氧气的质量:39.4g-34.6g=4.8g
总共收集到氧气的质量:9.6g+4.8g=14.4g
(2)设氯酸钾的总质量为x
2KClO3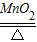 2KCl+3O2↑
2KCl+3O2↑
245 96
x 14.4g
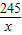 =
=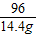
x=36.75g
二氧化锰的质量=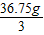 =12.25g
=12.25g
答:(1)该同学总共收集到氧气14.4g;
(2)最多能回收到二氧化锰12.25g.
点评:根据反应的化学方程式可以表示反应中各物质的质量比,由反应中某物质的质量可计算出反应中其它物质的质量.
(2)利用反应的化学方程式,由二次所收集氧气的总质量计算出所加氯酸钾的质量,根据用质量比为3:1的氯酸钾和二氧化锰制取氧气,求出加入的二氧化锰的质量;根据二氧化碳是催化剂剂在反应前后质量不变,收集到的二氧化锰的质量即所加入二氧化锰的质量.
解答:解:(1)第一次收集到氧气的质量:6.72L×1.429g/L=9.6g
第二次(充分加热)收集到氧气的质量:39.4g-34.6g=4.8g
总共收集到氧气的质量:9.6g+4.8g=14.4g
(2)设氯酸钾的总质量为x
2KClO3
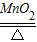 2KCl+3O2↑
2KCl+3O2↑245 96
x 14.4g
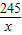 =
=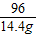
x=36.75g
二氧化锰的质量=
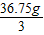 =12.25g
=12.25g答:(1)该同学总共收集到氧气14.4g;
(2)最多能回收到二氧化锰12.25g.
点评:根据反应的化学方程式可以表示反应中各物质的质量比,由反应中某物质的质量可计算出反应中其它物质的质量.

练习册系列答案
相关题目