题目内容
【题目】关于氧气的探究实验.
化学兴趣小组的同学用下图装置进行实验,实验步骤见表,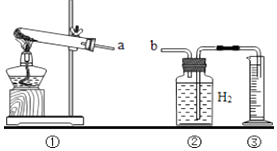
(1)请填空:
实验步骤 | 简答 |
(1)称取3g氯酸钾后与少量二氧化锰混合再装入装置①的试管中 | 装置①的试管中发生反应式: |
(2)加热试管一段时间后,用橡皮管连接a、b. | 刚开始加热时,排出的气体不宜立即收集,原因是: ② |
(3)当装置②中水面不再下降,断开a,b,移去酒精灯,将装置②中的集气瓶密封,并贴上标签备用. | |
(4)读取量筒里水的体积数并记录. | 读数时视线必须与凹液面的 ③ 保持水平. |
在理解上述实验的基础上,请你归纳本实验的目的:(不超过20个字) ④ .
(2)我们了解到常见制取氧气的方法有如图所示的四种: 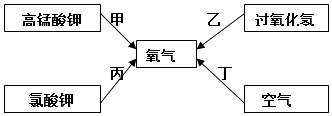
请回答问题:
①工业制取氧气的方法是(填“甲、乙、丙、丁”);下图标有字母“a”的仪器名称是 .
②用甲方法制取并收集氧气时,你将选用下图装置中的 , 若说明集气瓶中已充满氧气,反应式为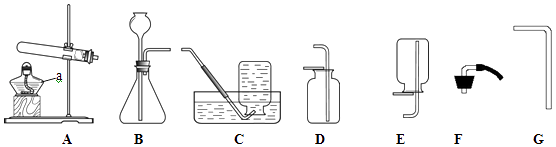
(3)某化学兴趣小组的同学,利用乙方法制取氧气,探究如下.
①把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并用排气法收集氧气,完成该实验你所选用的仪器有(填图中字母),写出化学反应式 , 该反应叫做;以上操作与“把二氧化锰加入盛有过氧化氢溶液的试管中制氧气”相比的优点是 .
②该小组继续探究“红砖粉末是否可以作为过氧化氢分解反应的催化剂?”实验如下:
a.分别向两支试管中加入相同的过氧化氢溶液,其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,结果发现加入红砖粉末的试管中反应较快.
b.将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
c.用称量后的固体重复步骤a的实验,现象与步骤a完全相同.
请回答:步骤a中除了选用试管外,还用到上面的仪器(填字母).步骤c的实验目的是 . 该小组学生认为上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为实验还缺少一个步骤,请指出该步骤是 .
【答案】
(1)2KClO3  2KCl+3O2↑|此时出现的气泡是空气而不是氧气|最低处|测定3g氯酸钾所产生的氧气的体积.
2KCl+3O2↑|此时出现的气泡是空气而不是氧气|最低处|测定3g氯酸钾所产生的氧气的体积.
(2)丁;酒精灯;AC或AD;瓶口处有气泡逸出或瓶口处带火星的木条复燃;2KMnO4  K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(3)BD;2H2O2 ![]() 2H2O+O2↑;分解反应;可以得到平稳的气流;FG;检验化学性质;测定反应前红砖粉末的质量
2H2O+O2↑;分解反应;可以得到平稳的气流;FG;检验化学性质;测定反应前红砖粉末的质量
【解析】解:(1)①氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,故填:2KClO3  2KCl+3O2↑;②刚开始冒出的气泡是空气而不是氧气,故刚有气泡冒出不能立刻收集,故填:此时出现的气泡是空气而不是氧气;③读数时,视线要平视凹液面的最低处,故填:最低处;④根据上述实验可以看出,该实验的目的是想测定3g氯酸钾所产生的氧气的体积,故填:测定3g氯酸钾所产生的氧气的体积;(2)①工业上采用分离液态空气的方法制取氧气,故是丁方法,据图可以看出,仪器a是酒精灯,故填:丁;酒精灯;②加热高锰酸钾制取氧气,是固体加热型反应,故发生装置是A,可以使用排水法或是向上排空气法收集,排水法收集时若是观察到瓶口有气泡产生,则收集满,使用向上排空气法,若是放在集气瓶口的带火星的木条复燃,则已经收集满,故填:AC或AD;若瓶口处有气泡逸出或瓶口处带火星的木条复燃;2KMnO4
2KCl+3O2↑;②刚开始冒出的气泡是空气而不是氧气,故刚有气泡冒出不能立刻收集,故填:此时出现的气泡是空气而不是氧气;③读数时,视线要平视凹液面的最低处,故填:最低处;④根据上述实验可以看出,该实验的目的是想测定3g氯酸钾所产生的氧气的体积,故填:测定3g氯酸钾所产生的氧气的体积;(2)①工业上采用分离液态空气的方法制取氧气,故是丁方法,据图可以看出,仪器a是酒精灯,故填:丁;酒精灯;②加热高锰酸钾制取氧气,是固体加热型反应,故发生装置是A,可以使用排水法或是向上排空气法收集,排水法收集时若是观察到瓶口有气泡产生,则收集满,使用向上排空气法,若是放在集气瓶口的带火星的木条复燃,则已经收集满,故填:AC或AD;若瓶口处有气泡逸出或瓶口处带火星的木条复燃;2KMnO4 ![]() K2MnO4+MnO2+O2↑;(3)①使用过氧化氢溶液制取氧气,是固液常温型反应,发生装置选择B,该反应是一种物质生成两种物质的分解反应,把过氧化氢溶液缓缓加入盛有二氧化锰的容器中可以得到平稳的气流,故填:BD;分解反应;2H2O2
K2MnO4+MnO2+O2↑;(3)①使用过氧化氢溶液制取氧气,是固液常温型反应,发生装置选择B,该反应是一种物质生成两种物质的分解反应,把过氧化氢溶液缓缓加入盛有二氧化锰的容器中可以得到平稳的气流,故填:BD;分解反应;2H2O2 ![]() 2H2O+O2↑;可以得到平稳的气流.②将试管中的气体导出通入水中,比较产生气泡的快慢,还需要的仪器是FG;步骤c的实验目的是检验化学性质;要证明是不是催化剂,还需要证明反应前后红砖粉的质量不变,故填:FG;检验化学性质;测定反应前红砖粉末的质量.
2H2O+O2↑;可以得到平稳的气流.②将试管中的气体导出通入水中,比较产生气泡的快慢,还需要的仪器是FG;步骤c的实验目的是检验化学性质;要证明是不是催化剂,还需要证明反应前后红砖粉的质量不变,故填:FG;检验化学性质;测定反应前红砖粉末的质量.
【考点精析】利用氧气的制取装置和氧气的收集方法对题目进行判断即可得到答案,需要熟知发生装置:固固加热型、固液不加热型;收集装置:根据物质的密度、溶解性;排水法收集时,待气泡均匀连续冒出时再收集(刚开始排出的是试管中的空气;)用排空气法收集气体时,导管伸到集气瓶底部.

 阅读快车系列答案
阅读快车系列答案