题目内容
25克含碳酸钙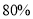 的大理石恰好与100克某盐酸溶液完全反应
的大理石恰好与100克某盐酸溶液完全反应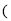 杂质不与盐酸反应,且不溶解
杂质不与盐酸反应,且不溶解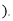 求:
求:
(1)生成二氧化碳的质量;
(2)原盐酸溶液的溶质质量分数;
(3)反应后溶液的质量.
练习册系列答案
相关题目
以下实验操作均正确的一组是( )
项目 | 进行的实验 | 所用试剂及主要实验操作 |
A | CO中除去CO2 | 通过装有足量NaOH溶液的洗气瓶后,干燥 |
B | 鉴别磷矿粉和硫酸铵两种化肥 | 观察颜色,灰白色固体物质为磷矿粉。白色晶体为硫酸铵 |
C | NaC1固体中除去CaCl2固体 | 加入适量K2CO3溶液,充分后,过滤、蒸发、结晶 |
D | Na2CO3固体中除去NaCl固体 | 溶于足量水中加入适量稀盐酸,蒸发结晶 |
A.A B.B C.C D.D
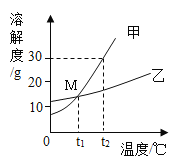
如表为氯化钠和氯化铵在不同温度时的溶解度,请回答下列问题。
温度/°C | 0 | 10 | 20 | 30 | 40 | 50 |
NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 49.6 |
NaC1溶解度/g | 35.4 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(1)由表中数据可知,溶解度随温度变化较大的物质是_____。
(2)20°C时,100g水最多能溶解NaC1_____g;
(3)向烧杯中加入100g水和49.0g氯化铵配成50°C的溶液,此时溶液为_____溶液(填“饱和”或“不饱和”);再冷却到20°C,烧杯中析出固体的质量为_____g;另外多角度看物质,有助于加深对物质的认识。Na2CO3是一种常见的盐,请回答:
(4)Na2CO3溶液显碱性,其pH_____7(填“<”、“>”或“=”);
(5)Na2CO3可看成是碱和氧化物反应的产物,写出反应的化学方程式_____。
(6)Na2CO3作为反应物之一,写出一个符合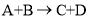 形式的化学方程式_____。
形式的化学方程式_____。


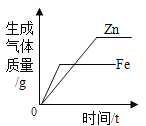 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应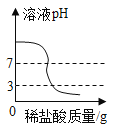 向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸
向一定量的氢氧化钠溶液中滴加pH=3的稀盐酸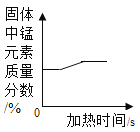 加热一定质量的高锰酸钾
加热一定质量的高锰酸钾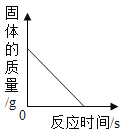 氢气还原一定质量的氧化铜
氢气还原一定质量的氧化铜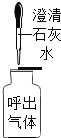 呼出气体中CO2比吸入空气中含量高 B.
呼出气体中CO2比吸入空气中含量高 B.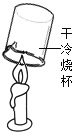 蜡烛中含氢元素
蜡烛中含氢元素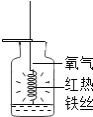 红热的铁丝在氧气中能燃烧 D.
红热的铁丝在氧气中能燃烧 D. 试管1中产生的是H2
试管1中产生的是H2