题目内容
为控制大气中“温室效应”(CO2、CH4)气体的排放量,“低碳”正成为人们的共识。
(1)近几十年来大气中二氧化碳含量不断上升的主要原因是 。
(2)生活中燃烧等物质的量的碳、一氧化碳、甲烷,最终排放出的二氧化碳的量 (选填编号)
A.一样多 B.碳多 C.一氧化碳多 D.甲烷多
(3)CO2常用来做灭火剂,但是遇到特殊物质时,CO2也能支持燃烧,写出镁条在CO2中燃烧的化学方程式 ,该反应中做还原剂的是 。
(4)实验室制取二氧化碳,采用的实验原理用化学方程式表示为 ;
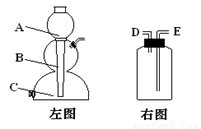
若用左图制取CO2则碳酸钙固体应该放置的位置是 ,若用右图收集CO2则气体进入的导管口应该是 (以上均用图中英文编号填写)。
(5)实验室利用澄清石灰水检验CO2时发生的化学方程式为 。
(1)燃烧煤炭、石油等矿物燃料
(2)A
(3)2Mg+CO2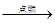 2MgO+C
Mg
2MgO+C
Mg
(4)CaCO3+2HCl→CaCl2+H2O+CO2↑ B )E
(5)CO2+Ca(OH)2→CaCO3↓+H2O
【解析】
试题分析:近几十年来由于燃烧煤炭、石油等矿物燃料燃料量增大,大气中二氧化碳含量不断上升;由于相同物质的量的的碳、一氧化碳和甲烷中含有相同物质的量的碳,根据质量守恒定律以上三种物质中的碳完全燃烧后都生成了二氧化碳,所以它们完全燃烧后都生成了相同物质的量的二氧化碳;镁在二氧化碳中燃烧生成氧化镁和碳,其中镁夺走了二氧化碳中的氧,发生了氧化反应是还原剂;实验室制是以石灰石和稀盐酸为原料制取二氧化碳的,该反应的生成物是氯化钙、水和二氧化碳,应根据以上信息书写化学方程式;若用启普发生器制取二氧化碳等气体,固体应放在B处;由于二氧化碳的密度比空气大若用右图装置收集气体,应从E端进入;二氧化碳与澄清石灰水中的溶质氢氧化钙发生化学反应生成碳酸钙沉淀和水,根据这些信息书写化学方程式。
考点:二氧化碳的来源、检验,化学方程式的书写和计算,氧气-还原反应。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案 为控制大气中“温室效应”(CO2、CH4)气体的排放量,“低碳”正成为人们的共识.
为控制大气中“温室效应”(CO2、CH4)气体的排放量,“低碳”正成为人们的共识. ④实验室制取二氧化碳,采用的实验原理用化学方程式表示为(5) ;
④实验室制取二氧化碳,采用的实验原理用化学方程式表示为(5) ;