题目内容
【题目】下列图象与所对应操作相符的是( )
A.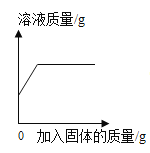 ①常温下,向饱和的硝酸钾溶液中加入硝酸钾
①常温下,向饱和的硝酸钾溶液中加入硝酸钾
B.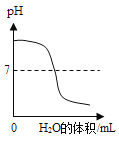 ②是对氢氧化钠溶液加水稀释
②是对氢氧化钠溶液加水稀释
C.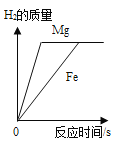 ③是将足量镁片和铁片分别和等量、等溶质质量分数的稀硫酸混合
③是将足量镁片和铁片分别和等量、等溶质质量分数的稀硫酸混合
D.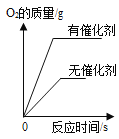 ④是用等质量、等浓度的双氧水分别制取氧气
④是用等质量、等浓度的双氧水分别制取氧气
【答案】C
【解析】
A.根据饱和溶液的概念来分析;
B.根据碱性溶液稀释后仍显碱性来分析;
C.根据金属与酸的反应过程来分析;
D.根据催化剂的概念来分析。
A.常温下,向饱和的硝酸钾溶液中加入硝酸钾,硝酸钾不会继续溶解,即溶液的质量不变,故错误;
B.氢氧化钠溶液加水稀释的过程中,碱性减弱,但是仍显碱性,即溶液的pH始终大于7,故错误;
C.将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合,由于金属是足量的,产生的氢气根据酸进行计算,由于酸是等质量、等溶质质量分数的,所以产生氢气相同,由于镁比铁活泼,所以镁反应得快,先到达最高点,故正确;
D.催化剂只能改变化学反应的速率,不能改变生成物的量,所以用等质量、等浓度的双氧水分别制取氧气,最终生成氧气的量相等,故错误。
故选:C。

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
【题目】合金的种类很多,用途非常广泛,黄铜是铜和锌的合金,它可以用来制造机器和电器的零件等,化学兴趣小组的同学欲测定实验室中某铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。
称量10g粉末状黄铜样品放入烧杯中,量取45mL稀盐酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | |
加入稀盐酸的体积(ml) | 15 | 15 | 15 |
生成氢气的质量(g) | 0.04 | m | 0.02 |
试求:
(1)m的数值 。
(2)此黄铜样品中铜的质量分数是多少?(写出计算过程)