题目内容
【题目】根据如示实验分析得的结论,不正确的是( )

A. 说明二氧化碳与水反应生成碳酸 B. 说明水是由氢元素和氧元素组成
C. 不同物质着火点不同 D. 黄铜的硬度比纯铜的大
【答案】A
【解析】本题主要考查二氧化碳的化学性质;电解水实验;燃烧与燃烧的条件。做题时可根据二氧化碳能溶于水及碳酸的酸性证明方法;水通电分解生成氢气和氧气;研究燃烧的条件,通过控制变量的方法做对比实验等分析。
A、将二氧化碳倒入盛水的塑料瓶中,拧紧瓶盖后瓶子变瘪,只能证明二氧化碳溶于水或和水反应,不能证明二氧化碳和水反应生成碳酸,应该通过加入紫色的石蕊试液变成红色证明,故不能达到实验目的;
B、水通电分解生成氢气和氧气,氢气是由氢元素组成,氧气是由氧元素组成,所以可证明水是由氢元素和氧元素组成的,故能达到实验目的;
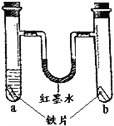
C、铜片的白磷燃烧,红磷不燃烧,能证明燃烧与温度是否达到可燃物的着火点有关,故能达到目的;
D、通过在纯铜片上的刻画,软的留下痕迹。故能达到实验目的
故选:A

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目