题目内容
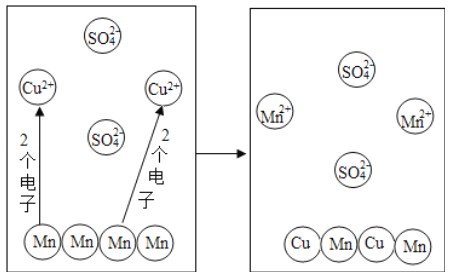
【题目】向一定质量AgNO3和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法正确的是( )

A. 取A点溶液,滴加稀盐酸,无白色沉淀
B. 图标上B~C段质量增加的原因是Zn与Cu(NO3)2溶液反应
C. B点时溶液中金属离子有Zn2+、Cu2+,金属单质有Zn、Cu、Ag
D. C点和D点溶质种类不同,金属单质种类也不同
【答案】B
【解析】试题分析:根据金属活动性顺序可知:锌先与硝酸银反应生成银和硝酸锌;此反应溶液质量减少,对应图像中的起点到b点段;A、a点处硝酸银还未完全反应,所以加盐酸时会反应生成硝酸银沉淀(白色)。此项不正确。B然后锌再与硝酸铜反应生成铜和硝酸锌;此反应溶液质量增加,对应图像中的b点到c点段;此项正确。C、b点为硝酸银恰好完全反应,所以溶液的成分为硝酸铜和硝酸锌;而固体成分为未反应的锌和生成的银;此项不正确。D、c点反应不再发生;所以cd点溶质相同。此项不正确。所以应选B项。

【题目】小明同学想在实验室用NaOH溶液与CO2气体制取Na2CO3溶液。但是经过检验,发现很难得到纯净的Na2CO3溶液,在老师的帮助下查阅了相关资料,制定了计划。
【查阅资料】
①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象。
②NaHCO3溶液煮沸时不会发生分解反应;NaHCO3溶液与CaCl2溶液不反应
③NaHCO3+NaOH=Na2CO3+H2O
④Na2CO3+CaCl2=CaCO3↓+2NaCl
【制取步骤】
①量取两份50 mL相同浓度的NaOH溶液备用;
②用一份50 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
③小心煮沸②溶液1-2分钟;
④在得到的③的溶液中加入另一份50 mL NaOH溶液,使其充分混合即得。
【实验探究】制得的Na2CO3溶液中可能含有的杂质是___________。
为检验制得的溶液是否为纯净的Na2CO3溶液,请你与小明同学一起完成下列实验探究:
实验步骤 | 实验现象 | 实验结论 | |
取少量制得的溶液于试管中,加入过量的显中性的CaCl2溶液 | ________。 | 溶液中含有Na2CO3 | |
将上步实验所得混合物进行过滤,将滤液分成两份 | 取其中一份加入足量的____, | 无气泡产生 | 制得的溶液中不含_____, |
取另一份加入______, |
| 制得的溶液中含NaOH | |
【结论】所制得的不是纯净的Na2CO3溶液。
【评价与反思】小芳同学认为可以用过量的Ca(OH)2溶液替代CaCl2溶液进行以上实验,你认为是否可行,并说明原因_______________。