题目内容
将11.4克生铁投入到足量的稀盐酸中充分反应后生成0.4克气体,则生铁中铁的质量分数是多少?
解:设生铁中铁的质量为X
Fe+2HCl═FeCl2+H2↑
56 2
X 0.4g
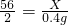 解得:X=11.2g
解得:X=11.2g
生铁中铁的质量分数是 ×100%=98.2%
×100%=98.2%
答:生铁中铁的质量分数是98.2%.
分析:根据铁与盐酸反应生成的氢气的质量可求出铁的质量,由铁的质量就可求出生铁中铁的质量分数.
点评:本题主要考查学生运用化学方程式和质量分数公式解答问题的能力.
Fe+2HCl═FeCl2+H2↑
56 2
X 0.4g
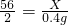 解得:X=11.2g
解得:X=11.2g生铁中铁的质量分数是
 ×100%=98.2%
×100%=98.2%答:生铁中铁的质量分数是98.2%.
分析:根据铁与盐酸反应生成的氢气的质量可求出铁的质量,由铁的质量就可求出生铁中铁的质量分数.
点评:本题主要考查学生运用化学方程式和质量分数公式解答问题的能力.

练习册系列答案
相关题目