题目内容
【题目】过氧化钠 (Na2O2 )是钠在氧气或空气中燃烧的产物之一, 白色, 能与二氧化碳反应放出氧气, 化学方程式为2Na2O2+2CO2=2Na2CO3+O2↑ 根据以上信息某同学用下列装置制取干燥氧气,请你回答问題:
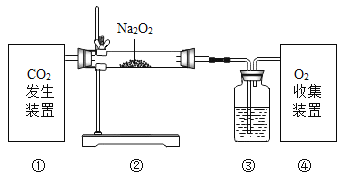
(1)装置①中是用稀盐酸和石灰石制取CO2,应选择是发生装置为________________(选填下图字母)该装置的气密性检查方法是___________________________________________________。
(2)装置③中盛装的试剂为_______________________。
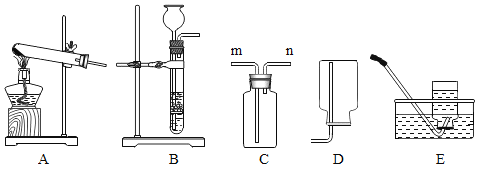
(3)若用装置A加热高锰酸钾固体来制取O2,该反应的化学方程式为_____________________。
(4)④为收集O2的装置,若用C装置收集,则气体从_____________(填“m”或“n ”)端通入·
【答案】B 橡皮管用止水夹夹住,从长颈漏斗中倒入水至淹没下端管口,使长颈漏斗中形成一段水柱,过一会,水柱不下降证明气密性良好 氢氧化钠溶液 2KMnO4![]() K2MnO4 + MnO2+O2↑ m
K2MnO4 + MnO2+O2↑ m
【解析】
(1)实验室制取CO2 ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;B装置的气密性检查方法是:橡皮管用止水夹夹住,从长颈漏斗中倒入水至淹没下端管口,使长颈漏斗中形成一段水柱,过一会,水柱不下降证明气密性良好;故填:B;橡皮管用止水夹夹住,从长颈漏斗中倒入水至淹没下端管口,使长颈漏斗中形成一段水柱,过一会,水柱不下降证明气密性良好。
(2)装置③中盛装的试剂为氢氧化钠溶液,是为了除去二氧化碳,故填:氢氧化钠溶液。
(3)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学方程式为2KMnO4![]() K2MnO4 + MnO2+O2↑,故填:2KMnO4
K2MnO4 + MnO2+O2↑,故填:2KMnO4![]() K2MnO4 + MnO2+O2↑。
K2MnO4 + MnO2+O2↑。
(4)若用C装置收集,因为氧气的密度比空气大,则气体从长管进入,故填:m。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】过氧化钠(![]() )是化学中常见的物质,为白至淡黄色的粉末状固体,易吸潮。与水发生反应生成氢氧化钠和具有氧化性的过氧化氢。
)是化学中常见的物质,为白至淡黄色的粉末状固体,易吸潮。与水发生反应生成氢氧化钠和具有氧化性的过氧化氢。
(1)写出过氧化钠与水的反应化学方程式 _____.
(2)为了验证过氧化钠与水反应生成了氢氧化钠,实验小组的同学将无色酚酞溶液滴到反应后的溶液中,观察到溶液变红又褪为无色。
(提出问题)什么原因使无色酚酞变红又褪色?
(猜想假设)小军:可能是无色酚酞溶液变质导致溶液褪色;
小敏:可能是氧气导致溶液褪色;
小花:_____.
(实验探究)A.小组同学都觉得小军的猜想不合理,原因_____.
B.小组同学用以下实验验证小敏和小花的猜想:
实验步骤 | 实验现象 | 实验结论 |
_____ | 无色酚酞溶液依然为红色 | 小敏猜想不正确 |
取少量稀氢氧化钠溶液于试管中,滴加 | _____ | 小花猜想正确 |